Văn bản hợp nhất 7/VBHN-BYT năm 2021 hợp nhất Thông tư quy định về quản lý mỹ phẩm do Bộ Y tế ban hành
Văn bản hợp nhất 7/VBHN-BYT năm 2021 hợp nhất Thông tư quy định về quản lý mỹ phẩm do Bộ Y tế ban hành
| Số hiệu: | 7/VBHN-BYT | Loại văn bản: | Văn bản hợp nhất |
| Nơi ban hành: | Bộ Y tế | Người ký: | Trương Quốc Cường |
| Ngày ban hành: | 16/03/2021 | Ngày hiệu lực: | Đã biết |
| Ngày công báo: | Đang cập nhật | Số công báo: | Đang cập nhật |
| Tình trạng: | Đã biết |
| Số hiệu: | 7/VBHN-BYT |
| Loại văn bản: | Văn bản hợp nhất |
| Nơi ban hành: | Bộ Y tế |
| Người ký: | Trương Quốc Cường |
| Ngày ban hành: | 16/03/2021 |
| Ngày hiệu lực: | Đã biết |
| Ngày công báo: | Đang cập nhật |
| Số công báo: | Đang cập nhật |
| Tình trạng: | Đã biết |
|
BỘ Y TẾ |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: 7/VBHN-BYT |
Hà Nội, ngày 16 tháng 03 năm 2021 |
Thông tư số 06/2011/TT-BYT ngày 25 tháng 01 năm 2011 của Bộ trưởng Bộ Y tế quy định về quản lý mỹ phẩm, có hiệu lực kể từ ngày 01 tháng 04 năm 2011 được sửa đổi, bổ sung bởi:
Thông tư số 29/2020/TT-BYT ngày 31 tháng 12 năm 2020 của Bộ trưởng Bộ Y tế sửa đổi, bổ sung và bãi bỏ một số văn bản quy phạm pháp luật do Bộ trưởng Bộ Y tế ban hành, liên tịch ban hành, có hiệu lực thi hành kể từ ngày 15 tháng 02 năm 2021.
Căn cứ Nghị định số 188/2007/NĐ-CP ngày 27 tháng 12 năm 2007 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Căn cứ Nghị định số 132/2008/NĐ-CP ngày 31 tháng 12 năm 2008 của Chính phủ quy định chi tiết thi hành một số điều của Luật Chất lượng sản phẩm, hàng hóa;
Căn cứ Nghị định số 24/2003/NĐ-CP ngày 13 tháng 3 năm 2003 của Chính phủ quy định chi tiết thi hành Pháp lệnh Quảng cáo;
Căn cứ Nghị định số 89/2006/NĐ-CP ngày 30 tháng 8 năm 2006 của Chính phủ quy định về ghi nhãn hàng hóa;
Căn cứ Nghị định số 12/2006/NĐ-CP ngày 23 tháng 01 năm 2006 của Chính phủ Quy định chi tiết thi hành Luật Thương mại về hoạt động mua bán hàng hóa quốc tế và các hoạt động đại lý mua, bán, gia công và quá cảnh hàng hóa với nước ngoài;
Căn cứ Quyết định số 10/2010/QĐ-TTg ngày 10 tháng 02 năm 2010 của Thủ tướng Chính phủ quy định Giấy chứng nhận lưu hành tự do đối với sản phẩm, hàng hóa xuất khẩu và nhập khẩu;
Để triển khai Hiệp định hòa hợp trong quản lý mỹ phẩm đã được các nước thành viên Hiệp hội các nước Đông Nam Á ký ngày 02 tháng 9 năm 2003 (gọi tắt là Hiệp định mỹ phẩm ASEAN), Bộ Y tế quy định về quản lý mỹ phẩm như sau:1
Điều 1. Phạm vi điều chỉnh và đối tượng áp dụng
1. Thông tư này quy định việc quản lý các sản phẩm mỹ phẩm sản xuất trong nước, mỹ phẩm nhập khẩu để lưu thông trong phạm vi lãnh thổ Việt Nam, bao gồm: công bố sản phẩm mỹ phẩm; hồ sơ thông tin sản phẩm; yêu cầu về an toàn sản phẩm; ghi nhãn mỹ phẩm; quảng cáo mỹ phẩm; xuất khẩu, nhập khẩu mỹ phẩm; lấy mẫu mỹ phẩm để kiểm tra chất lượng; kiểm tra, thanh tra và xử lý vi phạm; trách nhiệm của tổ chức, cá nhân sản xuất, buôn bán, nhập khẩu mỹ phẩm và quyền của người tiêu dùng.
2. Thông tư này áp dụng đối với các cơ quan quản lý nhà nước về mỹ phẩm, các tổ chức, cá nhân tiến hành các hoạt động liên quan đến công bố sản phẩm mỹ phẩm, thông tin, quảng cáo, xuất khẩu, nhập khẩu, sản xuất, buôn bán sản phẩm mỹ phẩm tại Việt Nam.
Trong Thông tư này các từ ngữ dưới đây được hiểu như sau:
1. Sản phẩm mỹ phẩm là một chất hay chế phẩm được sử dụng để tiếp xúc với những bộ phận bên ngoài cơ thể con người (da, hệ thống lông tóc, móng tay, móng chân, môi và cơ quan sinh dục ngoài) hoặc răng và niêm mạc miệng với mục đích chính là để làm sạch, làm thơm, thay đổi diện mạo, hình thức, điều chỉnh mùi cơ thể, bảo vệ cơ thể hoặc giữ cơ thể trong điều kiện tốt.
2. Tên mỹ phẩm là tên được đặt cho một sản phẩm mỹ phẩm, có thể là tên mới tự đặt cùng với thương hiệu hoặc tên của nhà sản xuất. Các ký tự cấu thành tên sản phẩm phải là các ký tự có gốc chữ cái Latin.
3. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường là tổ chức, cá nhân đứng tên trên hồ sơ công bố sản phẩm mỹ phẩm và chịu trách nhiệm về sản phẩm mỹ phẩm đó trên thị trường.
4. Số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm là số do cơ quan quản lý nhà nước có thẩm quyền cấp khi tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm. Số tiếp nhận Phiếu công bố có giá trị chứng nhận sản phẩm mỹ phẩm đã được tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường khai báo với cơ quan quản lý nhà nước có thẩm quyền về việc mỹ phẩm sẽ được lưu thông trên thị trường mà không có giá trị chứng nhận sản phẩm đó đảm bảo tính an toàn, hiệu quả, đáp ứng tất cả các yêu cầu của Hiệp định mỹ phẩm ASEAN và các phụ lục (Annexes) kèm theo.
5. Chủ sở hữu sản phẩm mỹ phẩm là tổ chức, cá nhân sở hữu công thức, quy trình sản xuất, tiêu chuẩn chất lượng sản phẩm.
6. Độ ổn định của sản phẩm là khả năng ổn định của sản phẩm khi được bảo quản trong điều kiện thích hợp vẫn duy trì được những tính năng ban đầu của nó, đặc biệt là vẫn phải đảm bảo được các yêu cầu về tính an toàn.
7. Định lượng của hàng hóa là lượng mỹ phẩm được thể hiện bằng khối lượng tịnh hoặc thể tích thực theo hệ mét hoặc cả hệ mét và hệ đo lường Anh.
8. Nhãn mỹ phẩm là bản viết, bản in, bản vẽ, bản chụp của chữ, hình vẽ, hình ảnh được dán, in, đính, đúc, chạm, khắc trực tiếp trên hàng hóa, bao bì thương phẩm của hàng hóa hoặc trên các chất liệu khác được gắn trên hàng hóa, bao bì thương phẩm của hàng hóa.
9. Ghi nhãn mỹ phẩm là thể hiện nội dung cơ bản, cần thiết về mỹ phẩm lên nhãn để người dùng nhận biết, làm căn cứ lựa chọn và sử dụng đúng; để nhà sản xuất, kinh doanh quảng bá cho hàng hóa của mình và làm căn cứ để các cơ quan chức năng thực hiện việc kiểm tra, kiểm soát.
10. Nhãn gốc là nhãn thể hiện lần đầu được gắn trên bao bì thương phẩm của mỹ phẩm.
11. Nhãn phụ là nhãn thể hiện những nội dung bắt buộc được dịch từ nhãn gốc của mỹ phẩm bằng tiếng nước ngoài ra tiếng Việt và bổ sung những nội dung bắt buộc bằng tiếng Việt theo quy định của Thông tư này mà nhãn gốc của mỹ phẩm còn thiếu.
12. Bao bì thương phẩm của mỹ phẩm là bao bì chứa đựng mỹ phẩm và lưu thông cùng với mỹ phẩm. Bao bì thương phẩm của mỹ phẩm gồm hai loại: Bao bì trực tiếp và bao bì ngoài.
a) Bao bì trực tiếp là bao bì chứa đựng hàng hóa, tiếp xúc trực tiếp với hàng hóa, tạo ra hình khối hoặc bọc kín theo hình khối của hàng hóa.
b) Bao bì ngoài là bao bì dùng để bao gói một hoặc một số đơn vị hàng hóa có bao bì trực tiếp.
13. Lưu thông mỹ phẩm là hoạt động trưng bày, vận chuyển, lưu giữ hàng hóa trong quá trình mua bán hàng hóa, trừ trường hợp vận chuyển hàng hóa của tổ chức, cá nhân nhập khẩu hàng hóa từ cửa khẩu về kho lưu giữ.
14. Số lô sản xuất mỹ phẩm là ký hiệu bằng số hoặc bằng chữ, hoặc kết hợp cả số và chữ nhằm nhận biết lô sản phẩm và cho phép truy xét toàn bộ lai lịch của một lô sản phẩm bao gồm tất cả các công đoạn của quá trình sản xuất, kiểm tra chất lượng và phân phối lô sản phẩm đó.
15. Ngày sản xuất mỹ phẩm là mốc thời gian hoàn thành sản xuất, chế biến, đóng gói hoặc các hình thức khác để hoàn thiện công đoạn cuối cùng của lô sản phẩm.
16. Hạn dùng của mỹ phẩm (hạn sử dụng) là mốc thời gian được ấn định cho một lô mỹ phẩm mà sau thời hạn này mỹ phẩm không được phép lưu thông, sử dụng.
17. Sử dụng tốt nhất trước ngày là mốc thời gian mà nhà sản xuất khuyên dùng khi chất lượng sản phẩm đang đạt mức tối ưu.
18. Xuất xứ hàng hóa của mỹ phẩm là nước hoặc vùng lãnh thổ nơi sản xuất ra toàn bộ mỹ phẩm hoặc nơi thực hiện công đoạn chế biến cơ bản cuối cùng đối với mỹ phẩm trong trường hợp có nhiều nước hoặc vùng lãnh thổ tham gia vào quá trình sản xuất mỹ phẩm đó.
19. Giấy chứng nhận lưu hành tự do (CFS - Certificate of Free Sale) là giấy chứng nhận do cơ quan có thẩm quyền của nước xuất khẩu cấp cho thương nhân xuất khẩu mỹ phẩm ghi trong CFS để chứng nhận rằng mỹ phẩm đó được sản xuất và được phép lưu hành tự do tại nước xuất khẩu.
20. Hướng dẫn sử dụng là những thông tin cần thiết để hướng dẫn cho người sử dụng mỹ phẩm an toàn, hợp lý. Hướng dẫn sử dụng có thể in trên bao bì trực tiếp hoặc theo dạng tài liệu đi kèm theo bao bì thương phẩm của mỹ phẩm trong đó ghi hướng dẫn sử dụng và những nội dung khác theo quy định.
21. Quảng cáo mỹ phẩm là các hoạt động giới thiệu, quảng bá mỹ phẩm nhằm thúc đẩy quá trình sản xuất, bán, sử dụng mỹ phẩm.
22. Hội thảo, sự kiện giới thiệu mỹ phẩm là hội nghị để giới thiệu hoặc thảo luận chuyên đềvới người tiêu dùng về các vấn đề chuyên sâu liên quan đến mỹ phẩm.
23. Người quảng cáo là tổ chức, cá nhân có nhu cầu quảng cáo về mỹ phẩm do mình sản xuất, phân phối.
24. Người phát hành quảng cáo là tổ chức, cá nhân đ ưa sản phẩm quảng cáo mỹ phẩm đến người tiêu dùng, bao gồm cơ quan báo chí, truyền thanh, truyền hình, nhà xuất bản, tổ chức quản lý mạng thông tin máy tính, người tổ chức chương trình văn hoá, thể thao, hội chợ, triển lãm và tổ chức, cá nhân sử dụng phương tiện quảng cáo khác.
25. Hội đồng mỹ phẩm ASEAN là cơ quan đại diện cho các nước thành viên ASEAN để theo dõi, quyết định và giải quyết các tranh chấp liên quan đến việc thực hiện Hiệp định mỹ phẩm ASEAN.
Điều 3. Quy định về việc công bố sản phẩm mỹ phẩm
1. Các tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường chỉ được phép đưa mỹ phẩm ra lưu thông khi đã được cơ quan quản lý nhà nước có thẩm quyền cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm và phải hoàn toàn chịu trách nhiệm về tính an toàn, hiệu quả và chất lượng sản phẩm. Cơ quan nhà nước có thẩm quyền sẽ tiến hành kiểm tra hậu mại khi sản phẩm lưu thông trên thị trường.
2. Lệ phí công bố sản phẩm mỹ phẩm được thực hiện theo quy định hiện hành.
3. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra lưu thông trên thị trường phải có chức năng kinh doanh mỹ phẩm tại Việt Nam.
4. Việc công bố tính năng của sản phẩm mỹ phẩm (mục đích sử dụng của sản phẩm) phải đáp ứng hướng dẫn của ASEAN về công bố tính năng sản phẩm mỹ phẩm (Phụ lục số 03-MP).
Điều 4. Hồ sơ công bố sản phẩm mỹ phẩm
Hồ sơ công bố sản phẩm mỹ phẩm bao gồm các tài liệu sau:
1. Phiếu công bố sản phẩm mỹ phẩm (02 bản) kèm theo dữ liệu công bố (bản mềm của Phiếu công bố);
2.2 (được bãi bỏ);
3. Bản chính hoặc bản sao có chứng thực hợp lệ Giấy ủy quyền của nhà sản xuất hoặc chủ sở hữu sản phẩm ủy quyền cho tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường được phân phối sản phẩm mỹ phẩm tại Việt Nam (áp dụng đối với mỹ phẩm nhập khẩu và mỹ phẩm sản xuất trong nước mà tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường không phải là nh à sản xuất). Đối với sản phẩm nhập khẩu thì Giấy ủy quyền phải là bản có chứng thực chữ ký và được hợp pháp hoá lãnh sự theo quy định của pháp luật, trừ trường hợp được miễn hợp pháp hoá lãnh sự theo các điều ước quốc tế mà Việt Nam là thành viên. Giấy ủy quyền phải đáp ứng các yêu cầu quy định tại Điều 6 Thông tư này.
4.3 Giấy chứng nhận lưu hành tự do (CFS) đối với sản phẩm mỹ phẩm nhập khẩu được quy định như sau:
a) Trường hợp miễn CFS bao gồm:
- Sản phẩm mỹ phẩm được sản xuất tại nước thành viên Hiệp định Đối tác Toàn diện và Tiến bộ xuyên Thái Bình Dương mà việc tham gia Hiệp định này đã được cơ quan có thẩm quyền của nước đó phê chuẩn và có hiệu lực (sau đây viết tắt là nước thành viên CPTPP);
- Sản phẩm mỹ phẩm được lưu hành và xuất khẩu từ nước thành viên CPTPP: Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường phải nộp tài liệu chứng minh sản phẩm được lưu hành tại nước thành viên CPTPP do cơ quan có thẩm quyền nước thành viên CPTPP cấp (giấy phép lưu hành sản phẩm mỹ phẩm hoặc phiếu công bố sản phẩm mỹ phẩm đã được cấp số tiếp nhận hoặc văn bản pháp lý khác có chứng nhận sản phẩm được lưu hành tại nước thành viên CPTPP) được hợp pháp hoá lãnh sự theo quy định của pháp luật, trừ trường hợp giấy tờ pháp lý thuộc một trong các trường hợp sau đây:
+ Được miễn hợp pháp hoá lãnh sự theo điều ước quốc tế mà nước Cộng hòa xã hội chủ nghĩa Việt Nam (sau đây viết tắt là Việt Nam) là thành viên hoặc theo nguyên tắc có đi có lại giữa Việt Nam và quốc gia cấp;
+ Được cơ quan ngoại giao nước ngoài hoặc cơ quan quản lý nhà nước về mỹ phẩm có thẩm quyền hoặc cơ quan cấp giấy tờ pháp lý của nước thành viên CPTPP gửi văn bản hoặc thư điện tử đến Cục Quản lý Dược xác nhận giấy tờ pháp lý;
+ Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường gửi kết quả tự tra cứu giấy tờ pháp lý từ trang thông tin điện tử (website tiếng Anh) của cơ quan cấp giấy tờ pháp lý của nước thành viên CPTPP có đóng dấu xác nhận của doanh nghiệp kèm theo văn bản cung cấp thông tin về đường dẫn tra cứu đến Cục Quản lý Dược. Doanh nghiệp phải chịu trách nhiệm trước pháp luật về tính hợp pháp, tính chính xác của các giấy tờ, thông tin này và kết quả tự tra cứu của doanh nghiệp;
- Sản phẩm mỹ phẩm đã được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm tại nước thuộc Hiệp hội các quốc gia Đông Nam Á (ASEAN): Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường phải nộp Phiếu công bố sản phẩm mỹ phẩm đã được cấp số tiếp nhận tại nước thuộc ASEAN được hợp pháp hoá lãnh sự theo quy định của pháp luật, trừ trường hợp Phiếu công bố sản phẩm mỹ phẩm thuộc một trong các trường hợp sau đây:
+ Được miễn hợp pháp hoá lãnh sự theo điều ước quốc tế mà nước Cộng hòa xã hội chủ nghĩa Việt Nam là thành viên hoặc theo nguyên tắc có đi có lại giữa Việt Nam và quốc gia cấp;
+ Được cơ quan ngoại giao nước ngoài hoặc cơ quan quản lý nhà nước về mỹ phẩm có thẩm quyền hoặc cơ quan cấp Phiếu công bố sản phẩm mỹ phẩm 3 của nước thành viên ASEAN gửi văn bản hoặc thư điện tử đến Cục Quản lý Dược xác nhận Phiếu công bố sản phẩm mỹ phẩm;
+ Doanh nghiệp chịu trách nhiệm đưa sản phẩm ra thị trường gửi kết quả tự tra cứu Phiếu công bố sản phẩm mỹ phẩm từ website tiếng Anh của cơ quan quản lý có thẩm quyền của nước thành viên ASEAN cấp số Phiếu tiếp nhận công bố sản phẩm mỹ phẩm có đóng dấu xác nhận của doanh nghiệp kèm theo văn bản cung cấp thông tin về đường dẫn tra cứu đến Cục Quản lý Dược. Doanh nghiệp phải chịu trách nhiệm trước pháp luật về tính hợp pháp, tính chính xác của các giấy tờ, thông tin này và kết quả tự tra cứu của doanh nghiệp;
b) Ngoài các trường hợp miễn CFS quy định tại điểm a khoản này, hồ sơ công bố sản phẩm mỹ phẩm nhập khẩu phải có CFS đáp ứng các yêu cầu sau đây:
- CFS do cơ quan có thẩm quyền của nước sản xuất hoặc nước xuất khẩu mỹ phẩm vào Việt Nam cấp còn thời hạn hiệu lực (bản chính hoặc bản sao chứng thực). Trường hợp CFS không nêu thời hạn thì phải là bản được cấp trong vòng 24 tháng kể từ ngày cấp;
- CFS phải được hợp pháp hoá lãnh sự theo quy định của pháp luật, trừ trường hợp CFS đáp ứng một trong các quy định sau đây:
+ Được miễn hợp pháp hóa lãnh sự theo điều ước quốc tế mà Việt Nam là thành viên hoặc theo nguyên tắc có đi có lại giữa Việt Nam và quốc gia cấp;
+ Có văn bản hoặc thư điện tử do cơ quan có thẩm quyền cấp CFS hoặc cơ quan ngoại giao nước ngoài gửi đến Cục Quản lý Dược có nội dung xác nhận thông tin của CFS;
- CFS phải có tối thiểu các thông tin quy định tại Điều 36 Luật quản lý ngoại thương và khoản 3 Điều 10 Nghị định số 69/2018/NĐ-CP ngày 15 tháng 5 năm 2018 của Chính phủ quy định chi tiết một số điều của Luật quản lý ngoại thương (sau đây gọi tắt là Nghị định số 69/2018/NĐ-CP).
Điều 5. Cách lập Phiếu công bố sản phẩm mỹ phẩm và dữ liệu công bố
1. Phiếu công bố sản phẩm mỹ phẩm:
a) Phiếu công bố sản phẩm mỹ phẩm được lập theo mẫu Phụ lục số 01-MP. Phiếu công bố phải được người đại diện theo pháp luật ký, có đóng dấu giáp lai của tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường. Cách ghi các nội dung trong Phiếu công bố sản phẩm mỹ phẩm theo hướng dẫn tại Phụ lục số 02-MP.
b) Mỗi sản phẩm mỹ phẩm được công bố trong một Phiếu công bố.
Sản phẩm mỹ phẩm được sản xuất hoàn chỉnh tại mỗi công ty sản xuất khác nhau thì công bố riêng. Trường hợp có trên một công ty tham gia các công đoạn sản xuất để sản xuất ra một sản phẩm hoàn chỉnh thì lập chung tron g một Phiếu công bố và phải nêu rõ tên và địa chỉ đầy đủ của từng công ty.
Các sản phẩm cùng một chủ sở hữu sản phẩm thuộc một trong các trường hợp sau đây được phép công bố trong một Phiếu công bố:
- Các sản phẩm được đóng dưới tên chung và được bán dưới dạng một bộ sản phẩm.
- Các sản phẩm cùng tên, cùng dòng sản phẩm có công thức tương tự nhau nhưng có màu sắc hoặc mùi khác nhau. Đối với sản phẩm nhuộm tóc, nước hoa công bố riêng cho từng màu, mùi.
- Các dạng khác sẽ được Cục Quản lý dược - Bộ Y tế quyết định dựa vào quyết định của Hội đồng mỹ phẩm ASEAN.
c) Cách ghi thành phần công thức có trong sản phẩm mỹ phẩm:
- Thành phần có trong công thức sản phẩm phải được ghi đầy đủ theo thứ tự hàm lượng giảm dần. Các thành phần nước hoa, chất tạo hương và cá c nguyên liệu của chúng có thể viết dưới dạng “hương liệu” (perfume, fragrance, flavour, aroma). Những thành phần với hàm lượng nhỏ hơn 1% có thể liệt kê theo bất kỳ thứ tự nào sau các thành phần có hàm lượng lớn hơn 1%. Các chất màu có thể được ghi theo bất cứ thứ tự nào sau các thành phần khác theo chỉ dẫn màu (CI) hoặc theo tên như trong Phụ lục IV (Annex IV) của Hiệp định mỹ phẩm ASEAN. Những sản phẩm mỹ phẩm dùng để trang điểm, dưới dạng các màu khác nhau có thể liệt kê tất cả các chất màu trong mục “có thể chứa” hoặc “+/-”.
- Nêu đầy đủ tỷ lệ phần trăm của các thành phần có quy định về giới hạn nồng độ, hàm lượng tại các Phụ lục (Annexes) của Hiệp định mỹ phẩm ASEAN. Giữa hàng đơn vị và hàng thập phân được đánh dấu bằng dấu phẩy (“,”).
- Tên thành phần phải được ghi bằng danh pháp quốc tế (International Nomenclature of Cosmetic Ingredients - INCI) quy định trong các ấn phẩm mới nhất: Từ điển thành phần mỹ phẩm quốc tế (International Cosmetic Ingredient Dictionary), Dược điển Anh (British Pharmacopoeia), Dược điển Mỹ (United States Pharmacopoeia), Dữ liệu tóm tắt về hoá học (Chemical Abstract Services), Tiêu chuẩn Nhật Bản về thành phần nguyên liệu mỹ phẩm (Japanese Standard Cosmetic Ingredient), Ấn phẩm của Nhật Bản về thành phần nguyên liệu mỹ phẩm (Japanese Cosmetic Ingredients Codex). Tên thực vật và dịch chiết từ thực vật phải được viết bằng tên khoa học bao gồm chi, loài thực vật (tên chi thực vật có thể rút ngắn). Các thành phần có nguồn gốc từ động vật cần nêu chính xác tên khoa học của loài động vật đó.
Những chất sau đây không được coi là thành phần của mỹ phẩm:
- Tạp chất trong nguyên liệu được sử dụng.
- Các nguyên liệu phụ được sử dụng vì mục đích kỹ thuật nhưng không có mặt trong sản phẩm thành phẩm.
- Nguyên liệu được sử dụng với số lượng cần thiết như dung môi hoặc chất mang của các thành phần tạo mùi.
d) Ngôn ngữ trình bày trong Phiếu công bố là tiếng Việt hoặc tiếng Anh. Các nội dung ghi tại mục 3 (Mục đích sử dụng), mục 7 (Thông tin về tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường), mục 8 (Thông tin về người đại diện theo pháp luật của Công ty), mục 9 (Thông tin về Công ty nhập khẩu) trong Phiếu công bố phải ghi bằng tiếng Việt hoặc tiếng Việt và tiếng Anh.
2. Dữ liệu công bố (bản mềm của Phiếu công bố): Các tổ chức, cá nhân có thể nộp dữ liệu công bố quy định tại khoản 1 Điều 4 của Thông tư này theo một trong hai cách thức sau:
a) Khai báo trực tiếp: Tổ chức, cá nhân đứng tên công bố sản phẩm mỹ phẩm gửi văn bản về Cục Quản lý dược - Bộ Y tế để được cấp tài khoản truy cập vào cơ sở dữ liệu về quản lý mỹ phẩm, khai báo trực tiếp trên cơ sở dữ liệu. Phiếu công bố nộp cho cơ quan quản lý nhà nước có thẩm quyền phải được in ra từ cơ sở dữ liệu đó.
b) Truy cập vào trang thông tin điện tử của Cục Quản lý dược, tải cơ sở dữ liệu của Phiếu công bố sản phẩm mỹ phẩm (Phụ lục số 01-MP), điền đầy đủ thông tin theo quy định vào cơ sở dữ liệu, sao lưu vào phương tiện lưu giữ điện tử (USB, CD-ROM, ...). Phiếu công bố nộp cho cơ quan quản lý nhà nước có thẩm quyền phải được in ra từ cơ sở dữ liệu đó.
Tổ chức, cá nhân đứng tên công bố sản phẩm phải chịu hoàn toàn trách nhiệm về tính phù hợp các nội dung của Phiếu công bố sản phẩm mỹ phẩm (bản có ký tên, đóng dấu) với dữ liệu công bố (bản mềm) đã khai báo hoặc nộp cho cơ quan quản lý.
Điều 6. Quy định về Giấy ủy quyền
1. Ngôn ngữ trình bày là tiếng Việt, tiếng Anh hoặc song ngữ tiếng Việt và tiếng Anh.
2. Giấy ủy quyền phải có đầy đủ các nội dung sau:
a) Tên, địa chỉ của nhà sản xuất; trường hợp bên ủy quyền là chủ sở hữu sản phẩm thì cần nêu rõ tên, địa chỉ của chủ sở hữu sản phẩm và tên, địa chỉ của nhà sản xuất;
b) Tên, địa chỉ của tổ chức, cá nhân được ủy quyền;
c) Phạm vi ủy quyền (đứng tên công bố và phân phối sản phẩm mỹ phẩm tại Việt Nam);
d) Nhãn hàng hoặc tên sản phẩm được ủy quyền;
đ) Thời hạn ủy quyền;
e) Cam kết của nhà sản xuất hoặc chủ sở hữu sản phẩm cung cấp đầy đủ Hồ sơ thông tin sản phẩm (PIF) cho tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường tại Việt Nam;
g) Tên, chức danh, chữ ký của người đại diện cho bên ủy quyền.
Điều 7. Thủ tục tiếp nhận và giải quyết hồ sơ công bố sản phẩm mỹ phẩm
1. Hồ sơ công bố sản phẩm mỹ phẩm được làm thành 01 bộ, nộp trực tiếp hoặc gửi qua đường bưu điện tới cơ quan quản lý nhà nước có thẩm quyền sau:
a) Đối với mỹ phẩm nhập khẩu: Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường nộp hồ sơ công bố sản phẩm mỹ phẩm tại Cục Quản lý dược - Bộ Y tế.
b) Đối với mỹ phẩm sản xuất trong nước: Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường nộp hồ sơ công bố sản phẩm mỹ phẩm tại Sở Y tế nơi đặt nhà máy sản xuất. Sản phẩm mỹ phẩm được sản xuất, đóng gói từ bán thành phẩm nhập khẩu được coi như sản phẩm sản xuất trong nước.
c) Đối với mỹ phẩm kinh doanh trong phạm vi Khu thương mại công nghiệp thuộc Khu kinh tế cửa khẩu Mộc Bài, tỉnh Tây Ninh thực hiện công bố tại Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài; mỹ phẩm kinh doanh trong phạm vi Khu kinh tế - thương mại đặc biệt Lao Bảo, tỉnh Quảng Trị thực hiện công bố tại Ban Quản lý Khu kinh tế tỉnh Quảng Trị.
Việc đưa mỹ phẩm từ Khu thương mại công nghiệp thuộc Khu kinh tế cửa khẩu Mộc Bài, tỉnh Tây Ninh vào các khu chức năng khác trong Khu kinh tế cửa khẩu Mộc Bài, tỉnh Tây Ninh hoặc đưa vào thị trường nội địa để kinh doanh; đưa mỹ phẩm từ Khu Kinh tế - Thương mại đặc biệt Lao Bảo, tỉnh Quảng Trị vào thị trường nội địa để kinh doanh phải thực hiện công bố tại Cục Quản lý dược - Bộ Y tế theo quy định của Thông tư này (tổ chức, cá nhân đứng tên công bố sản phẩm mỹ phẩm phải có chức năng kinh doanh mỹ phẩm tại Việt Nam và nằm ngoài 2 khu này).
2. Giải quyết hồ sơ công bố sản phẩm mỹ phẩm:
a) Trong vòng 03 ngày làm việc kể từ ngày nhận được hồ sơ công bố hợp lệ và lệ phí công bố theo quy định, cơ quan quản lý nhà nước có thẩm quyền có trách nhiệm ban hành số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
b) Trường hợp hồ sơ công bố chưa đáp ứng theo quy định của Thông tư này thì trong vòng 05 ngày làm việc kể từ ngày nhận được hồ sơ, cơ quan tiếp nhận hồ sơ thông báo bằng văn bản cho tổ chức, cá nhân công bố biết các nội dung chưa đáp ứng để sửa đổi, bổ sung hồ sơ (nêu cụ thể các nội dung chưa đáp ứng).
Hồ sơ bổ sung của đơn vị gồm:
- Văn bản giải trình về việc sửa đổi, bổ sung của tổ chức, cá nhân đứng tên công bố;
- Phiếu công bố sản phẩm mỹ phẩm kèm theo dữ liệu công bố (bản mềm của Phiếu công bố) hoặc tài liệu khác được sửa đổi, bổ sung;
Trong vòng 05 ngày làm việc kể từ ngày nhận được hồ sơ bổ sung đáp ứng theo quy định của Thông tư này, cơ quan quản lý nhà nước có thẩm quyền có trách nhiệm ban hành số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
Trường hợp hồ sơ sửa đổi, bổ sung không đáp ứng theo quy định của Thông tư này thì trong vòng 05 ngày làm việc kể từ ngày nhận được hồ sơ bổ sung, cơ quan tiếp nhận hồ sơ thông báo bằng văn bản không cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm cho sản phẩm này.
c) Trong thời gian 03 tháng kể từ ngày ban hành văn bản thông báo theo quy định tại điểm b khoản này, nếu cơ quan quản lý nhà nước có thẩm quyền không nhận được hồ sơ bổ sung của tổ chức, cá nhân đứng tên công bố thì hồ sơ công bố không còn giá trị. Trong trường hợp này, nếu tổ chức, cá nhân muốn tiếp tục công bố thì phải nộp hồ sơ mới và nộp lệ phí mới theo quy định.
Điều 8. Quy định về cách ghi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm
Số tiếp nhận phiếu công bố sản phẩm mỹ phẩm được quy định như sau: số thứ tự được cấp + gạch chéo + năm cấp (hai chữ số cuối) + gạch chéo + CBMP + gạch ngang + ký hiệu viết tắt tên tỉnh, thành phố, Ban Quản lý Khu kinh tế hoặc Cục Quản lý dược (QLD) theo Phụ lục số 04-MP.
Ví dụ: 135/11/CBMP-HN có nghĩa là số tiếp nhận Phiếu công bố mỹ phẩm là 135 do Sở Y tế Hà Nội cấp năm 2011.
Điều 9. Thay đổi các nội dung đã công bố
Đối với các sản phẩm mỹ phẩm đã công bố và được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm, khi có thay đổi các nội dung quy đ ịnh tại Phụ lục số 05-MP, tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải có văn bản đề nghị bổ sung (đối với các nội dung không phải công bố mới) kèm theo tài liệu có liên quan đến nội dung bổ sung và phải được sự chấp thuận bằng văn bản của cơ quan nhà nước có thẩm quyền hoặc thực hiện công bố mới theo quy định (đối với các nội dung phải công bố mới).
Điều 10. Hiệu lực của số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm
Số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm có giá trị 05 năm kể từ ngày cấp. Hết thời hạn 05 năm, tổ chức, cá nhân muốn tiếp tục đưa sản phẩm mỹ phẩm ra lưu thông trên thị trường thì phải công bố lại trước khi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm hết hạn và phải nộp lệ phí theo quy định.
HỒ SƠ THÔNG TIN SẢN PHẨM MỸ PHẨM
Điều 11. Quy định chung về Hồ sơ thông tin sản phẩm mỹ phẩm
Mỗi sản phẩm mỹ phẩm khi đưa ra lưu thông trên thị trường phải có Hồ sơ thông tin sản phẩm (PIF - Product Information File) theo hướng dẫn của ASEAN lưu giữ tại địa chỉ của tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường.
Điều 12. Nội dung của Hồ sơ thông tin sản phẩm mỹ phẩm
1. Hồ sơ Thông tin sản phẩm mỹ phẩm gồm có 4 phần như sau:
a) Phần 1: Tài liệu hành chính và tóm tắt về sản phẩm;
b) Phần 2: Chất lượng của nguyên liệu;
c) Phần 3: Chất lượng của thành phẩm;
d) Phần 4: An toàn và hiệu quả.
Nội dung chi tiết của Hồ sơ Thông tin sản phẩm mỹ phẩm quy định tại Phụ lục số 07-MP.
2. Phần 1 của Hồ sơ thông tin sản phẩm phải được xuất trình ngay cho cơ quan kiểm tra, thanh tra khi được yêu cầu; các phần khác nếu chưa đầy đủ thì xuất trình trong vòng 15-60 ngày kể từ ngày kiểm tra theo yêu cầu của cơ quan chức năng.
YÊU CẦU VỀ AN TOÀN SẢN PHẨM MỸ PHẨM
Điều 13. Yêu cầu về an toàn sản phẩm mỹ phẩm
Các tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường phải đảm bảo các sản phẩm của mình không có hại đối với sức khoẻ con người khi được dùng trong những điều kiện bình thường hoặc những điều kiện thích hợp được hướng dẫn, phù hợp với dạng bào chế, thông tin ghi trên nhãn, hướng dẫn sử dụng, thận trọng đặc biệt, cũng như các thông tin khác cung cấp bởi nhà sản xuất hoặc chủ sở hữu sản phẩm.
Nhà sản xuất, chủ sở hữu sản phẩm phải đánh giá tính an toàn trên mỗi sản phẩm mỹ phẩm theo Hướng dẫn đánh giá tính an toàn mỹ phẩm của ASEAN. Giới hạn kim loại nặng và vi sinh vật trong mỹ phẩm phải đáp ứng yêu cầu của ASEAN quy định tại Phụ lục số 06-MP. Thành phần công thức mỹ phẩm phải đáp ứng theo các Phụ lục (Annexes) - bản mới nhất của Hiệp định mỹ phẩm ASEAN (địa chỉ truy cập: www.dav.gov.vn hoặc www.aseansec.org).
Các tổ chức, cá nhân không được đưa ra thị trường những sản phẩm mỹ phẩm có chứa:
1. Các chất cấm sử dụng trong mỹ phẩm với điều kiện đi kèm được liệt kê trong Phụ lục II (Annex II).
2. Các thành phần được liệt kê trong phần thứ nhất của Phụ lục III (Annex III), với nồng độ, hàm lượng vượt quá giới hạn hoặc nằm ngoài điều kiện cho phép.
3. Các chất màu khác với các chất được liệt kê trong Phụ lục IV (Annex IV), phần 1, trừ trường hợp các mỹ phẩm chứa các chất màu với mục đích duy nhất để nhuộm tóc.
4. Các chất màu được liệt kê trong Phụ lục IV (Annex IV), phần 1 được sử dụng ngoài điều kiện đã nêu.
5. Các chất bảo quản nằm ngoài danh mục trong Phụ lục VI (Annex VI), phần 1.
6. Các chất bảo quản được liệt kê trong Phụ lục VI (Annex VI), phần 1, với hàm lượng vượt quá giới hạn hoặc nằm ngoài điều kiện cho phép, trừ trường hợp các chất này được sử dụng với mục đích đặc biệt, không liên quan đến công dụng là chất bảo quản.
7. Các chất lọc tia tử ngoại nằm ngoài danh mục trong Phụ lục VII (Annex VII), phần 1.
8. Các chất lọc tia tử ngoại nằm trong Phụ lục VII (Annex VII), phần 1 nhưng có hàm lượng vượt quá giới hạn hoặc điều kiện cho phép.
Sự có mặt của các chất được liệt kê trong Phụ lục II (Annex II) với hàm lượng vết vẫn được chấp nhận nếu vì lý do kỹ thuật không thể tránh được trong “Thực hành tốt sản xuất mỹ phẩm” và vẫn đảm bảo yêu cầu về độ an toàn của mỹ phẩm như quy định tại Điều 13 của Thông tư này.
1. Các thành phần hoặc nguyên liệu được liệt kê trong Phụ lục III (Annex III), phần 2, trong giới hạn và theo những điều kiện đã nêu, cho đến ngày được quy định trong cột (g) của Phụ lục này.
2. Các chất màu được liệt kê trong Phụ lục IV, phần 2, trong giới hạn cho phép và trong điều kiện được chấp nhận, cho đến ngày được quy định trong phụ lục này.
3. Các chất bảo quản được liệt kê trong Phụ lục VI, phần 2, trong giới hạn cho phép và trong điều kiện được chấp nhận, cho đến ngày được đề cập đến trong cột (f) của Phụ lục này. Tuy nhiên, một vài thành phần trong số này có thể được sử dụng ở những hàm lượng khác với mục đích cụ thể, được thể hiện rõ ràng trong dạng trình bày của sản phẩm.
4. Các chất lọc tia tử ngoại được quy định trong phần 2 của Phụ lục VII (Annex VII), trong giới hạn cho phép và trong điều kiện đã quy định, cho đến ngày được đề cập đến trong cột (f) của Phụ lục này.
Quy định về việc sử dụng các chất nằm trong các Phụ lục (Annexes) nêu trên có thể thay đổi theo quyết định của Hội đồng mỹ phẩm ASEAN. Các quy định này sẽ tự động được cập nhật và có giá trị tại Việt Nam.
1. Nhãn mỹ phẩm phải được gắn trên hàng hóa, bao bì thương phẩm của hàng hóa ở vị trí khi quan sát có thể nhận biết được dễ dàng, đầy đủ các nội dung quy định của nhãn mà không phải tháo rời các chi tiết, các phần của hàng hóa.
2. Trường hợp không được hoặc không thể mở bao bì ngoài thì trên bao bì ngoài phải có nhãn và nhãn phải trình bày đầy đủ các nội dung bắt buộc.
Điều 17. Kích thước, hình thức và nội dung của nhãn
1. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường tự xác định kích thước của nhãn hàng hóa mỹ phẩm nhưng phải bảo đảm thông tin ghi trên nhãn phải dễ đọc bằng mắt thường. Nội dung của nhãn và nhãn phụ (nếu có) phải trung thực, rõ ràng, chính xác và phản ánh đúng tính năng của sản phẩm.
2. Màu sắc của chữ, chữ số, hình vẽ, hình ảnh, dấu hiệu, ký hiệu trình bày trên nhãn mỹ phẩm phải rõ ràng. Màu sắc của chữ và số phải tương phản với nền của nhãn.
Điều 18. Nội dung bắt buộc phải ghi trên nhãn
1. Nhãn sản phẩm mỹ phẩm phải phù hợp với yêu cầu ghi nhãn mỹ phẩm của ASEAN.Những thông tin sau phải được thể hiện trên nhãn sản phẩm:
a) Tên của sản phẩm và chức năng của nó, trừ khi dạng trình bày sản phẩm đã thể hiện rõ ràng chức năng của sản phẩm;
b) Hướng dẫn sử dụng, trừ khi dạng trình bày đã thể hiện rõ ràng cách sử dụng của sản phẩm;
c) Thành phần công thức đầy đủ: Phải ghi rõ các thành phần theo danh pháp quốc tế quy định trong các ấn phẩm mới nhất nêu tại điểm c khoản 1 Điều 5 của Thông tư này (không phải ghi tỷ lệ phần trăm của các thành phần);
d) Tên nước sản xuất;
đ) Tên và địa chỉ của tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường (ghi đầy đủ bằng tiếng Việt theo Giấy chứng nhận đăng ký kinh doanh hoặc Giấy phép đầu tư);
e) Định lượng thể hiện bằng khối lượng tịnh hoặc thể tích, theo hệ mét hoặc cả hệ mét và hệ đo lường Anh;
g) Số lô sản xuất;
h) Ngày sản xuất hoặc hạn dùng phải được thể hiện một cách rõ ràng (ví dụ: ngày/tháng/năm). Cách ghi ngày phải thể hiện rõ ràng gồm tháng, năm hoặc ngày, tháng, năm theo đúng thứ tự. Có thể dùng từ “ngày hết hạn” hoặc “sử dụng tốt nhất trước ngày”, nếu cần thiết có thể bổ sung thêm điều kiện chỉ định cần tuân thủ để đảm bảo sự ổn định của sản phẩm.
Với những sản phẩm có độ ổn định dưới 30 tháng, bắt buộc phải ghi ngày hết hạn;
i) Lưu ý về an toàn khi sử dụng, đặc biệt theo những lưu ý nằm trong cột "Điều kiện sử dụng và những cảnh báo bắt buộc phải in trên nhãn sản phẩm" được đề cập trong các phụ lục của Hiệp định mỹ phẩm ASEAN, những thận trọng này bắt buộc phải thể hiện trên nhãn sản phẩm.
2. Trong trường hợp kích thước, dạng hoặc chất liệu bao gói không thể in được đầy đủ các thông tin quy định tại khoản 1 Điều này trên nhãn gốc, những nội dung bắt buộc này phải được ghi trên nhãn phụ đính kèm theo sản phẩm mỹ phẩm và trên nhãn mỹ phẩm phải chỉ ra nơi ghi các nội dung đó.
Các thông tin sau đây bắt buộc phải được ghi trên nhãn gốc của bao bì trực tiếp của sản phẩm:
a) Tên sản phẩm;
b) Số lô sản xuất.
Điều 19. Ngôn ngữ trình bày trên nhãn mỹ phẩm
Những nội dung quy định tại Điều 18 của Thông tư này phải được trình bày bằng tiếng Anh hoặc tiếng Việt; riêng các thông tin tại điểm b, đ, i khoản 1 Điều 18 phải ghi bằng tiếng Việt.
Điều 20. Các nội dung khác thể hiện trên nhãn mỹ phẩm
Tổ chức, cá nhân được phép ghi trên nhãn mỹ phẩm những nội dung khác. Những nội dung ghi thêm không được trái với quy định của pháp luật và phải đảm bảo trung thực, chính xác, phản ánh đúng bản chất của hàng hóa, không che khuất, không làm sai lệch những nội dung bắt buộc ghi trên nhãn mỹ phẩm.
Việc xuất khẩu mỹ phẩm thực hiện tại cơ quan Hải quan theo quy định pháp luật hiện hành và các yêu cầu của nước nhập khẩu.
Điều 33. Hồ sơ, thủ tục cấp Giấy chứng nhận lưu hành tự do (CFS) đối với mỹ phẩm sản xuất trong nước để xuất khẩu 5
1. Hồ sơ đề nghị cấp CFS đối với mỹ phẩm xuất khẩu thực hiện theo quy định tại Điều 11 Nghị định số 69/2018/NĐ-CP. Riêng bản Tiêu chuẩn công bố áp dụng đối với sản phẩm, hàng hóa có thể thay thế bằng Phiếu công bố sản phẩm mỹ phẩm đã được cấp số tiếp nhận (01 bản sao có đóng dấu của thương nhân).
2. Quy trình cấp CFS đối với mỹ phẩm xuất khẩu thực hiện theo quy định tại Điều 11 Nghị định số 69/2018/NĐ-CP.
3. Phí cấp CFS tính theo sản phẩm tương ứng với 01 Phiếu công bố sản phẩm mỹ phẩm đã được cấp số tiếp nhận.
4. Sở Y tế tỉnh, thành phố trực thuộc Trung ương thực hiện việc cấp và quản lý CFS đối với mỹ phẩm xuất khẩu được sản xuất trên địa bàn nơi đặt cơ sở sản xuất mỹ phẩm.
1. Đơn vị sản xuất có nhu cầu cấp Giấy chứng nhận cơ sở đáp ứng các nguyên tắc, tiêu chuẩn “Thực hành tốt sản xuất mỹ phẩm” của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN) để phục vụ cho xuất khẩu gửi hồ sơ đăng ký kiểm tra về Cục Quản lý dược - Bộ Y tế. Hồ sơ bao gồm:
a) Phiếu đăng ký kiểm tra “Thực hành tốt sản xuất mỹ phẩm” (Phụ lục số 13-MP);
b)6 (được bãi bỏ);
c) Sơ đồ tổ chức và nhân sự của cơ sở (sơ đồ tổ chức phải thể hiện rõ tên, chức danh, trình độ chuyên môn kỹ thuật của các cán bộ phụ trách các bộ phận), quá trình công tác và kinh nghiệm trong lĩnh vực được phân công của các cán bộ phụ trách các bộ phận (sản xuất, kiểm tra chất lượng, đảm bảo chất lượng, nhà kho);
d)7 (được bãi bỏ);
đ) Sơ đồ vị trí và thiết kế của nhà máy (bao gồm: sơ đồ mặt bằng tổng thể; sơ đồ đường đi của công nhân; sơ đồ đường đi của nguyên liệu, bao bì, bán thành phẩm, thành phẩm; sơ đồ hệ thống xử lý chất thải);
e) Danh mục thiết bị hiện có của nhà máy (bao gồm thiết bị sản xuất và thiết bị kiểm tra chất lượng mỹ phẩm) phải thể hiện được tên thiết bị, năm sản xuất, nước sản xuất và tình trạng của thiết bị;
g)8 (được bãi bỏ);
h) Biên bản tự thanh tra “Thực hành tốt sản xuất mỹ phẩm” (Biên bản tự thanh tra phải thể hiện rõ thời gian thanh tra, thành phần đoàn tự thanh tra, mục tiêu tự thanh tra, kết quả tự thanh tra và các đề xuất thời gian và biện pháp khắc phục các tồn tại).
2. Thẩm quyền tiếp nhận và giải quyết hồ sơ:
Cục Quản lý dược - Bộ Y tế có trách nhiệm xem xét hồ sơ, lên kế hoạch và ra quyết định thành lập đoàn kiểm tra, thông báo cho cơ sở ít nhất 10 ngày trước khi tiến hành kiểm tra.
3. Giấy chứng nhận cơ sở đáp ứng các nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất mỹ phẩm" có giá trị 03 năm kể từ ngày cấp.
4. Đơn vị sản xuất (gọi tắt là cơ sở đăng ký GMP) phải nộp phí thẩm định tiêu chuẩn và điều kiện sản xuất mỹ phẩm theo quy định hiện hành.
1.9 (được bãi bỏ).
2. Nhập khẩu mỹ phẩm trong một số trường hợp đặc biệt (không bắt buộc phải thực hiện công bố sản phẩm mỹ phẩm theo quy định của Thông tư này):
a) Tổ chức, cá nhân nhập khẩu mỹ phẩm để nghiên cứu, kiểm nghiệm phải gửi đơn hàng nhập khẩu mỹ phẩm dùng cho nghiên cứu, kiểm nghiệm tới Cục Quản lý dược - Bộ Y tế (Phụ lục số 14-MP). Số lượng tối đa cho mỗi sản phẩm là 10 mẫu.
Đơn hàng nhập khẩu mỹ phẩm dùng cho nghiên cứu, kiểm nghiệm được làm thành 03 bản. Sau khi được phê duyệt, 02 bản được lưu tại Cục Quản lý dược, 01 bản gửi đơn vị. Bản gửi đơn vị có đóng dấu “Bản gửi doanh nghiệp” để trình cơ quan Hải quan khi làm thủ tục thông quan.
Các sản phẩm mỹ phẩm nhập khẩu để nghiên cứu, kiểm nghiệm phải được sử dụng đúng mục đích, không được phép đưa ra lưu thông trên thị trường.
b) Tổ chức, cá nhân nhận mỹ phẩm là quà biếu, quà tặng làm thủ tục nhập khẩu tại cơ quan Hải quan theo quy định. Tổng trị giá mỗi lần nhận không vượt quá định mức hàng hóa được miễn thuế theo quy định hiện hành.
Các mẫu mỹ phẩm nhập khẩu là quà biếu, quà tặng không được phép đưa ra lưu thông trên thị trường.
c) Tổ chức, cá nhân nhập khẩu mỹ phẩm để trưng bày tại hội chợ, triển lãm và các trường hợp tạm nhập tái xuất khác phải làm thủ tục xin cấp giấy phép tạm nhập tái xuất của Bộ Công Thương theo quy định hiện hành.
LẤY MẪU MỸ PHẨM ĐỂ KIỂM TRA CHẤT LƯỢNG
1. Lấy mẫu mỹ phẩm để kiểm tra hoặc giám sát chất lượng theo nguyên tắc lấy mẫu ngẫu nhiên và phải lấy mẫu ở những vị trí khác nhau của lô hàng.
2. Lượng mẫu cần lấy để phân tích và để lưu căn cứ vào yêu cầu kiểm tra, tiêu chuẩn chất lượng, phương pháp thử nhưng ít nhất phải đủ cho ba lần ph ân tích hoặc phải đủ để thực hiện phép thử đảm bảo thu được kết quả chính xác và tin cậy.
3. Các mẫu phân tích và mẫu lưu phải được cho vào đồ đựng, hàn kín và dán nhãn. Nhãn của đồ đựng mẫu phải ghi rõ tên sản phẩm, tên tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường, số lô sản xuất, hạn dùng, nơi lấy mẫu, ngày lấy mẫu.
4. Lập biên bản lấy mẫu mỹ phẩm theo mẫu Phụ lục số 09-MP: Biên bản lấy mẫu mỹ phẩm phải ghi rõ tên sản phẩm, số lô sản xuất, ngày lấy mẫu, địa điểm lấy mẫu, ghi chép về những bất thường của quá trình lấy mẫu, tên và chữ ký của người lấy mẫu, đại diện cơ sở được lấy mẫu, người chứng kiến (khi cần thiết). Biên bản được làm thành 03 bản: một bản lưu tại cơ sở được lấy mẫu, một bản lưu tại cơ quan kiểm nghiệm, một bản lưu tại cơ quan quản lý kiểm tra chất lượng mỹ phẩm.
Điều 37. Quyền hạn và trách nhiệm của người lấy mẫu
1. Xuất trình thẻ thanh tra viên hoặc kiểm soát viên chất lượng hoặc giấy giới thiệu hoặc quyết định thành lập đoàn kiểm tra do thủ trưởng cơ quan kiểm tra chất lượng mỹ phẩm ký khi thi hành nhiệm vụ.
2. Yêu cầu cơ sở có mẫu xuất trình các hồ sơ, tài liệu, liên quan đến nguồn gốc, số lượng, chất lượng của lô mỹ phẩm được lấy mẫu, đưa ra phương án lấy mẫu, số lượng mẫu phân tích và mẫu lưu được lấy của lô mỹ phẩm trong quá trình lấy mẫu.
3. Kiểm tra, lấy mẫu bất kỳ bao gói nào trong lô mỹ phẩm khi có nghi ngờ về chất lượng, tính an toàn của sản phẩm.
4. Chịu trách nhiệm trước pháp luật về các thao tác kỹ thuật, thủ tục pháp lý trong quá trình lấy mẫu, vận chuyển và bàn giao mẫu cho cơ quan kiểm nghiệm.
Điều 38. Vận chuyển và bàn giao mẫu
1. Sau khi hoàn tất việc lấy mẫu, người lấy mẫu phải chuyển các mẫu đã lấy kèm biên bản lấy mẫu mỹ phẩm và bàn giao ngay cho cơ quan kiểm nghiệm. Trường hợp đặc biệt, mẫu có thể gửi đến cơ quan kiểm nghiệm qua đường bưu điện.
2. Mẫu mỹ phẩm đã lấy phải được đóng gói trong bao gói phù hợp và vận chuyển bằng phương tiện thích hợp để đảm bảo mẫu được bảo quản theo đúng quy định, tránh hư hỏng, đổ vỡ trong quá trình vận chuyển.
Điều 39. Kết luận kết quả kiểm tra chất lượng các mẫu mỹ phẩm
1. Các mẫu mỹ phẩm do các cơ quan nhà nước có thẩm quyền về kiểm tra chất lượng lấy mẫu đảm bảo tính đại diện cho cả lô mỹ phẩm và được tiến hành phân tích tại các phòng thử nghiệm được công nhận thì kết luận kết quả kiểm tra chất lượng có giá trị pháp lý đối với cả lô mỹ phẩm.
2. Các mẫu mỹ phẩm do tổ chức, cá nhân gửi tới cơ quan kiểm tra chất lượng của nhà nước để xác định chất lượng thì kết luận kết quả kiểm tra chất lượng chỉ có giá trị pháp lý đối với mẫu gửi tới.
Điều 40. Kinh phí lấy mẫu mỹ phẩm và kiểm nghiệm xác định chất lượng mỹ phẩm
1. Kinh phí lấy mẫu và kinh phí kiểm nghiệm mẫu mỹ phẩm để kiểm tra chất lượng trong sản xuất, pha chế và lưu thông trên thị trường do cơ quan kiểm tra chất lượng quyết định việc lấy mẫu và kiểm nghiệm mẫu chi trả theo quy định tại Thông tư liên tịch số 28/2010/TTLT-BTC-BKHCN ngày 03/3/2010 của liên bộ Tài chính và Khoa học và Công nghệ hướng dẫn quản lý và sử dụng kinh phí đối với hoạt động kiểm tra nhà nước về chất lượng sản phẩm, hàng hóa.
2. Trong trường hợp mẫu mỹ phẩm kiểm nghiệm được cơ quan kiểm tra chất lượng mỹ phẩm kết luận không đạt tiêu chuẩn chất lượng, tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải hoàn trả toàn bộ kinh phí lấy mẫu và kinh phí kiểm nghiệm mẫu mỹ phẩm cho cơ quan kiểm tra chất lượng theo quy định tại các Điều 10, Điều 12, Điều 14, Điều 16 và Điều 41 của Luật Chất lượng sản phẩm, hàng hóa năm 2007, Thông tư liên tịch số 28/2010/TTLT - BTC-BKHCN ngày 03/3/2010 của liên bộ Tài chính và Khoa học và Công nghệ hướng dẫn quản lý và sử dụng kinh phí đối với hoạt động kiểm tra nhà nước về chất lượng sản phẩm, hàng hóa và các văn bản quy phạm pháp luật có liên quan.
3. Trường hợp mỹ phẩm bị khiếu nại, tố cáo về chất lượng mà cơ quan kiểm tra kết luận việc khiếu nại, tố cáo về chất lượng mỹ phẩm không đúng thì người khiếu nại, tố cáo phải thanh toán hoàn trả chi phí lấy mẫu và chi phí phân tích, kiểm nghiệm mẫu mỹ phẩm cho cơ quan kiểm tra quy định tại khoản 1 Điều này.
4. Kinh phí lấy mẫu mỹ phẩm để kiểm tra chất lượng, kinh phí kiểm nghiệm mẫu mỹ phẩm được bố trí trong dự toán kinh phí hoạt động của cơ quan kiểm tra chất lượng nhà nước về mỹ phẩm theo quy định tại Thông tư liên tịch số 28/2010/TTLT-BTC-BKHCN ngày 03/3/2010 của liên bộ Tài chính và Khoa học và Công nghệ hướng dẫn quản lý và sử dụng kinh phí đối với hoạt động kiểm tra nhà nước về chất lượng sản phẩm, hàng hóa.
KIỂM TRA, THANH TRA VÀ XỬ LÝ VI PHẠM
Điều 41. Kiểm tra nhà nước về chất lượng mỹ phẩm
1. Cơ quan kiểm tra chất lượng mỹ phẩm:
a) Cơ quan kiểm tra chất lượng mỹ phẩm ở Trung ương là Cục Quản lý dược - Bộ Y tế. Cục Quản lý dược chỉ đạo hệ thống kiểm nghiệm trên phạm vi toàn quốc. Trong hoạt động kiểm tra nhà nước về chất lượng mỹ phẩm, Cục Quản lý dược phối hợp với Thanh tra Bộ Y tế, Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc thành phố Hồ Chí Minh, Sở Y tế các tỉnh, thành phố trực thuộc Trung ương triển khai và giám sát các hoạt động về hậu mại đối với các sản phẩm mỹ phẩm.
Trên cơ sở kết quả kiểm nghiệm mỹ phẩm của các cơ quan kiểm nghiệm nhà nước, Cục Quản lý dược - Bộ Y tế là cơ quan kết luận chất lượng mỹ phẩm trên phạm vi toàn quốc.
b) Cơ quan kiểm tra chất lượng mỹ phẩm ở địa phương là Sở Y tế tỉnh, thành phố trực thuộc Trung ương. Sở Y tế các tỉnh, thành phố Trung ương tổ chức triển khai các hoạt động về hậu mại đối với mỹ phẩm sản xuất trong nước, mỹ phẩm nhập khẩu lưu thông trên địa bàn và xử lý các vấn đề về chất lượng mỹ phẩm theo quy định của pháp luật. Theo dõi, thống kê tình hình quản lý chất lượng mỹ phẩm tại địa phương.
Kết luận chất lượng mỹ phẩm trên cơ sở kết quả kiểm nghiệm mỹ phẩm của cơ sở kiểm nghiệm nhà nước về mỹ phẩm tại địa phương.
2. Hệ thống kiểm nghiệm của nhà nước về mỹ phẩm bao gồm:
a) Ở Trung ương: Viện Kiểm nghiệm thuốc Trung ương, Viện Kiểm nghiệm thuốc thành phố Hồ Chí Minh;
b) Ở địa phương: Trung tâm kiểm nghiệm thuốc và mỹ phẩm các tỉnh, thành phố trực thuộc Trung ương.
3. Thủ trưởng các cơ quan kiểm nghiệm chất lượng mỹ phẩm chịu trách nhiệm về kết luận kết quả kiểm tra chất lượng mỹ phẩm trước pháp luật.
Điều 42. Hình thức kiểm tra, thanh tra
1. Kiểm tra, thanh tra định kỳ: Kiểm tra, thanh tra định kỳ sẽ được cơ quan có thẩm quyền thông báo trước cho đơn vị được kiểm tra để đơn vị chuẩn bị về việc thanh tra trước khi tiến hành hoạt động kiểm tra, thanh tra.
2. Kiểm tra, thanh tra đột xuất: Kiểm tra, thanh tra đột xuất khi phát hiện những sản phẩm không đạt chất lượng, không tuân thủ quy định lưu thông trên thị trường hoặc do các khiếu nại của khách hàng. Trong trường hợp khẩn cấp, cơ quan có thẩm quyền có quyền kiểm tra, thanh tra không cần báo trước.
Điều 43. Nội dung kiểm tra, thanh tra
1. Kiểm tra, thanh tra việc chấp hành pháp luật về sản xuất, buôn bán mỹ phẩm:
a) Việc tuân thủ các nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất mỹ phẩm" của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN) hoặc tương đương được Hội đồng mỹ phẩm ASEAN thừa nhận;
b) Ghi nhãn mỹ phẩm;
c) Hồ sơ thông tin sản phẩm (PIF) theo quy định của ASEAN;
d) Quảng cáo mỹ phẩm.
2. Kiểm tra, thanh tra việc giải quyết tranh chấp, khiếu nại, tố cáo về chất lượng và các nội dung khác liên quan đến mỹ phẩm (nếu có).
3. Kiểm tra, thanh tra việc thực hiện thông báo thu hồi mỹ phẩm theo quy định (nếu có).
Điều 44. Thứ tự ưu tiên trong kiểm tra giám sát hậu mại
Việc kiểm tra, thanh tra giám sát hậu mại mỹ phẩm cần tập trung tại các đơn vị nhập khẩu, phân phối, sản xuất. Thứ tự ưu tiên trong việc kiểm tra giám sát hậu mại mỹ phẩm dựa vào loại sản phẩm, nguồn gốc xuất xứ, nhãn hàng, thương hiệu công ty, thành phần công thức sản phẩm theo hướng dẫn của ASEAN về kiểm tra giám sát hậu mại (Phụ lục số 08-MP).
Điều 45. Đình chỉ lưu hành và thu hồi mỹ phẩm
1. Mỹ phẩm bị đình chỉ lưu hành và thu hồi khi xảy ra một trong các trường hợp sau:
a) Mỹ phẩm lưu thông khi chưa được cơ quan quản lý nhà nước có thẩm quyền cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm;
b) Mỹ phẩm không đạt chất lượng, không an toàn cho người sử dụng;
c) Mỹ phẩm lưu thông có công thức không đúng như hồ sơ đã công bố;
d) Mỹ phẩm lưu thông có chứa thành phần chất cấm sử dụng trong mỹ phẩm, các chất có nồng độ, hàm lượng vượt quá giới hạn cho phép;
đ) Mỹ phẩm lưu thông có nhãn ghi công dụng không phù hợp với hồ sơ công bố hoặc không đáp ứng quy định về ghi nhãn sản phẩm của Thông tư này, tùy mức độ vi phạm có thể bị đình chỉ lưu hành và thu hồi;
e) Mỹ phẩm lưu thông được sản xuất tại cơ sở không đáp ứng nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất mỹ phẩm" của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN) hoặc tương đương được Hội đồng mỹ phẩm ASEAN thừa nhận, tuỳ mức độ vi phạm có thể bị đình chỉ lưu hành và thu hồi;
g) Mỹ phẩm hết hạn sử dụng hoặc quá thời hạn theo khuyến cáo của nhà sản xuất;
h) Mỹ phẩm giả, nhập lậu, không rõ nguồn gốc, xuất xứ, mỹ phẩm không còn nguyên vẹn bao bì;
i) Mỹ phẩm do tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường có văn bản thu hồi tự nguyện.
2. Thẩm quyền ra quyết định thu hồi mỹ phẩm vi phạm:
a) Cục Quản lý dược - Bộ Y tế ra quyết định thu hồi mỹ phẩm vi phạm trong phạm vi toàn quốc.
b) Sở Y tế tỉnh, thành phố trực thuộc Trung ương, Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài (tỉnh Tây Ninh), Ban Quản lý Khu kinh tế tỉnh Quảng Trị thực hiện thông báo của Cục Quản lý dược - Bộ Y tế về thu hồi mỹ phẩm vi phạm theo quy định của pháp luật trên địa bàn và báo cáo về Cục Quản lý dược.
Điều 46. Thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm
1. Số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm bị thu hồi khi xảy ra một trong các trường hợp sau:
a) Mỹ phẩm lưu thông có 2 lô không đạt chất lượng do cơ quan quản lý nhà nước về chất lượng mỹ phẩm kết luận;
b) Mỹ phẩm lưu thông có công thức không đúng như hồ sơ đã công bố;
c) Mỹ phẩm lưu thông có nhãn ghi sai lệch nguồn gốc, xuất xứ;
d) Mỹ phẩm lưu thông có nhãn ghi sai lệch bản chất tính năng vốn có của sản phẩm;
đ) Mỹ phẩm không an toàn cho người sử dụng;
e) Mỹ phẩm lưu thông có chứa thành phần chất cấm sử dụng trong mỹ phẩm, các chất có nồng độ, hàm lượng vượt quá giới hạn cho phép;
g) Mỹ phẩm bị các cơ quan nhà nước có thẩm quyền kết luận là vi phạm quyền sở hữu trí tuệ hoặc mạo nhãn của sản phẩm khác đã được phép lưu hành;
h) Mỹ phẩm bị cấm lưu hành ở nước sở tại;
i) Tổ chức, cá nhân đưa sản phẩm ra thị trường có văn bản đề nghị thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm;
k) Không có Hồ sơ thông tin sản phẩm (PIF) xuất trình cho cơ quan có thẩm quyền theo quy định tại Điều 12 của Thông tư này;
l) Giả mạo tài liệu, sử dụng con dấu giả hoặc giả mạo chữ ký, dấu của cơ quan chức năng Việt Nam hoặc nước ngoài, của nhà sản xuất hoặc chủ sở hữu sản phẩm;
m) Kê khai không trung thực các nội dung trong Phiếu công bố sản phẩm mỹ phẩm.
2. Thẩm quyền ra quyết định thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm:
a) Cục Quản lý dược - Bộ Y tế ra quyết định thu hồi số tiếp nhận Phiếu công bố sản phẩm sản xuất trong nước do Cục Quản lý dược cấp số tiếp nhận trước ngày 25/4/2009, mỹ phẩm nhập khẩu trong phạm vi toàn quốc.
b) Sở Y tế tỉnh, thành phố trực thuộc Trung ương ra quyết định thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm sản xuất tại địa phương do đơn vị mình cấp.
c) Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài (tỉnh Tây Ninh), Ban Quản lý Khu kinh tế tỉnh Quảng Trị ra quyết định thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do đơn vị mình cấp.
1. Cơ quan quản lý nhà nước có thẩm quyền sẽ tạm ngừng xem xét và tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm 06 tháng đối với các tổ chức, cá nhân có một trong các hành vi sau:
a) Kinh doanh mỹ phẩm nhập lậu, mỹ phẩm giả, không rõ nguồn gốc, xuất xứ;
b) Kinh doanh mỹ phẩm chưa được cơ quan quản lý nhà nước có thẩm quyền cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm;
c) Không thực hiện thu hồi mỹ phẩm vi phạm theo thông báo của cơ quan nhà nước có thẩm quyền;
d) Sản xuất, kinh doanh mỹ phẩm tại cơ sở không tuân thủ các nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất mỹ phẩm" của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN) hoặc tương đương được Hội đồng mỹ phẩm ASEAN thừa nhận;
đ) Sản xuất, kinh doanh mỹ phẩm có thành phần chất cấm sử dụng trong mỹ phẩm hoặc vượt quá giới hạn cho phép đối với các chất có quy định giới hạn nồng độ, hàm lượng sử dụng theo quy định hiện hành của pháp luật;
e) Sử dụng nguyên liệu sản xuất mỹ phẩm đã bị nước sản xuất công bố cấm lưu thông trên thị trường;
g) Nhập khẩu, kinh doanh mỹ phẩm hoặc nguyên liệu sản xuất mỹ phẩm đã bị nước sản xuất công bố cấm lưu thông trên thị trường;
h) Sản xuất, kinh doanh mỹ phẩm có công thức không đúng như hồ sơ công bố;
i) Giả mạo tài liệu, sử dụng con dấu giả hoặc giả mạo chữ ký, dấu của cơ quan chức năng Việt Nam hoặc nước ngoài, của nhà sản xuất hoặc chủ sở hữu sản phẩm;
k) Kê khai không trung thực các nội dung trong Phiếu công bố sản phẩm mỹ phẩm;
l) Không có Hồ sơ thông tin sản phẩm (PIF) lưu tại doanh nghiệp theo quy định.
2. Cơ quan quản lý nhà nước có thẩm quyền sẽ tạm ngừng xem xét và tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm 06 tháng đối với tổ chức, cá nhân có một trong các hành vi sau:
a) Quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm khi chưa có Phiếu tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm do cơ quan quản lý nhà nước có thẩm quyền cấp theo quy định của pháp luật;
b) Quảng cáo mỹ phẩm hoặc tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm đối với các sản phẩm mỹ phẩm chưa được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm;
c) Quảng cáo mỹ phẩm có thể làm cho người tiêu dùng hiểu nhầm sản phẩm đó là thuốc; quảng cáo mỹ phẩm có sử dụng danh nghĩa, biểu tượng, hình ảnh, thư tín của tổ chức y, dược, của cán bộ y tế; quảng cáo mỹ phẩm nêu tính năng công dụng chưa đủ cơ sở khoa học.
3. Cơ quan quản lý nhà nước có thẩm quyền sẽ xem xét tạm ngừng tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm, hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm đối với tổ chức, cá nhân không nộp báo cáo kết quả hoạt động sản xuất kinh doanh hàng năm theo quy định.
Hết thời hạn tạm ngừng xem xét, tiếp nhận hồ sơ, sau khi đơn vị đã khắc phục đầy đủ các vi phạm và có báo cáo, cơ quan quản lý nhà nước có thẩm quyền sẽ tiếp tục xem xét, tiếp nhận hồ sơ công bố sản phẩm mỹ phẩm, hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu sản phẩm mỹ phẩm của đơn vị.
TRÁCH NHIỆM CỦA TỔ CHỨC, CÁ NHÂN SẢN XUẤT, BUÔN BÁN, NHẬP KHẨU MỸ PHẨM VÀ QUYỀN CỦA NGƯỜI TIÊU DÙNG
1. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường phải chịu hoàn toàn trách nhiệm về các nội dung kê khai trong Phiếu công bố sản phẩm mỹ phẩm, chịu hoàn toàn trách nhiệm về tính an toàn, hiệu quả và chất lượng sản phẩm, đảm bảo rằng sản phẩm đưa ra lưu thông đáp ứng tất cả các yêu cầu của Hiệp định mỹ phẩm ASEAN và các Phụ lục kèm theo.
2. Tổ chức, cá nhân đưa sản phẩm mỹ phẩm lưu hành trên thị trường có trách nhiệm theo dõi, phát hiện và thu hồi ngay mỹ phẩm không đạt tiêu chuẩn chất lượng, thực hiện thông báo thu hồi của cơ quan quản lý nhà nước có thẩm quyền, báo cáo về việc thu hồi mỹ phẩm gửi cơ quan nhà nước có thẩm quyền; giải quyết kịp thời khiếu nại của khách hàng về chất lượng mỹ phẩm, bồi thường thiệt hại cho khách hàng theo quy định của pháp luật. Đồng thời, phải hoàn trả lại tiền cho người mua hàng và các chi phí phát sinh trong quá trình bảo quản, vận chuyển, lưu thông sản phẩm.
3. Trường hợp phát hiện những tác dụng phụ trầm trọng ảnh hưởng đến tính mạng người tiêu dùng do chất lượng sản phẩm mỹ phẩm, tổ chức và cá nhân đưa sản phẩm ra thị trường phải báo cáo tới Cục Quản lý dược - Bộ Y tế trong vòng 07 ngày kể từ ngày nhận được thông tin đầu tiên về tác dụng phụ này theo mẫu tại Phụ lục số 18-MP. Báo cáo chi tiết về tác dụng phụ trầm trọng này phải được gửi về Cục Quản lý dược - Bộ Y tế trong vòng 08 ngày tiếp theo.
4. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải lưu giữ Hồ sơ thông tin sản phẩm (PIF) trong thời gian tối thiểu 03 năm kể từ khi lô sản xuất cuối cùng được đưa ra thị trường và xuất trình khi cơ quan chức năng kiểm tra, thanh tra yêu cầu.
5. Các đơn vị sản xuất mỹ phẩm phải triển khai áp dụng và đáp ứng các nguyên tắc, tiêu chuẩn "Thực hành tốt sản xuất mỹ phẩm" của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN).
6. Tổ chức, cá nhân kinh doanh mỹ phẩm phải thực hiện các yêu cầu của cơ quan nhà nước có thẩm quyền trong việc kiểm tra, thanh tra về chất lượng mỹ phẩm, thu hồi mỹ phẩm vi phạm và được quyền khiếu nại về kết luận và hình thức xử lý vi phạm theo quy định của pháp luật về khiếu nại, tố cáo.
7. Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải tuân thủ các quy định và luật pháp Việt Nam về sở hữu trí tuệ. Khi có kết luận của cơ quan nhà nước có thẩm quyền về nhãn hiệu, kiểu dáng công nghiệp vi phạm quyền sở hữu trí tuệ, tổ chức, cá nhân phải ngừng sản xuất, buôn bán, nhập khẩu để tiến hành thay đổi nhãn hiệu, kiểu dáng công nghiệp theo đúng quy định và có trách nhiệm bồi hoàn và xử lý hậu quả (nếu có).
Điều 49. Quyền của người tiêu dùng mỹ phẩm
Người tiêu dùng có quyền được thông tin về mỹ phẩm, có quyền khiếu nại, tố cáo và yêu cầu đơn vị kinh doanh mỹ phẩm bồi thường thiệt hại theo quy định của pháp luật do sử dụng mỹ phẩm sản xuất, lưu thông không đảm bảo chất lượng, không an toàn.
Điều 50. Thông tin và chế độ báo cáo
1. Cục Quản lý dược - Bộ Y tế có trách nhiệm cập nhật và triển khai các quy định liên quan đến Hiệp định mỹ phẩm ASEAN trên trang thông tin điện tử của Cục Quản lý dược (địa chỉ: www.dav.gov.vn). Thường xuyên phổ biến cho đơn vị có liên quan và các tổ chức, cá nhân sản xuất, kinh doanh mỹ phẩm các thay đổi về tiêu chí kỹ thuật đã được quyết định bởi Hội đồng mỹ phẩm ASEAN, đồng thời phối hợp triển khai các thay đổi và quyết định đó tại Việt Nam. Mọi quyết định về quản lý mỹ phẩm được thông qua bởi Hội đồng mỹ phẩm ASEAN được áp dụng tại Việt Nam.
2. Cục Quản lý dược, Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài (tỉnh Tây Ninh), Ban Quản lý Khu kinh tế tỉnh Quảng Trị có trách nhiệm đưa kết quả xử lý các hành vi vi phạm trong lĩnh vực mỹ phẩm theo thẩm quyền trên trang thông tin điện tử của cơ quan; có lộ trình đưa danh sách các sản phẩm mỹ phẩm đã cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm và những nội dung thông tin, quảng cáo mỹ phẩm đã giải quyết trên trang thông tin điện tử của cơ quan để phục vụ công tác kiểm tra, thanh tra, giám sát hậu mại.
3. Định kỳ vào ngày 30 tháng 6 và 31 tháng 12 hàng năm, Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài (tỉnh Tây Ninh), Ban Quản lý Khu kinh tế tỉnh Quảng Trị gửi báo cáo tình hình quản lý chất lượng và công tác hậu kiểm mỹ phẩm tại địa phương, báo cáo về việc cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm (Phụ lục số 15-MP), báo cáo về việc cấp Phiếu tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm (Phụ lục số 16-MP) về Cục Quản lý dược - Bộ Y tế.
4. Định kỳ ngày 30 tháng 01 hàng năm, tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải gửi báo cáo kết quả hoạt động sản xuất kinh doanh năm trước của đơn vị mình về Cục Quản lý dược - Bộ Y tế và Sở Y tế sở tại (Phụ lục số 17-MP).
Điều 51. Biểu mẫu, Phụ lục kèm theo Thông tư
1. Mẫu Phiếu công bố sản phẩm mỹ phẩm: Phụ lục số 01-MP.
2. Tài liệu hướng dẫn về công bố sản phẩm mỹ phẩm: Phụ lục số 02-MP.
3. Hướng dẫn của ASEAN về công bố tính năng của sản phẩm mỹ phẩm: Phụ lục số 03-MP.
4. Quy ước viết tắt tên các tỉnh, thành phố trực thuộc Trung ương và một số Ban Quản lý Khu kinh tế: Phụ lục số 04-MP.
5. Thay đổi sau khi công bố sản phẩm mỹ phẩm: Phụ lục số 05-MP.
6. Quy định của ASEAN về giới hạn kim loại nặng và vi sinh vật trong sản phẩm mỹ phẩm: Phụ lục số 06-MP.
7. Hồ sơ thông tin sản phẩm: Phụ lục số 07-MP.
8. Tài liệu hướng dẫn của ASEAN về kiểm tra hậu mại mỹ phẩm: Phụ lục số 08-MP.
9. Mẫu Biên bản lấy mẫu mỹ phẩm để kiểm tra chất lượng: Phụ lục số 09-MP.
10. Mẫu Phiếu đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm: Phụ lục số 10-MP.
11. Mẫu Phiếu tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm: Phụ lục số 11-MP.
12. Mẫu Giấy chứng nhận lưu hành tự do (CFS): Phụ lục số 12-MP.
13. Mẫu Phiếu đăng ký kiểm tra thực hành tốt sản xuất mỹ phẩm: Phụ lục số 13-MP.
14. Mẫu đơn hàng nhập khẩu dùng cho nghiên cứu, kiểm nghiệm: Phụ lục số 14-MP.
15. Mẫu báo cáo danh sách mỹ phẩm đã cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm: Phụ lục số 15-MP.
16. Mẫu báo cáo danh sách mỹ phẩm đã cấp Phiếu tiếp nhận hồ sơ đăng ký quảng cáo, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm: Phụ lục số 16-MP.
17. Mẫu báo cáo kết quả hoạt động sản xuất, kinh doanh mỹ phẩm: Phụ lục số 17-MP.
18. Mẫu thông báo tác dụng bất lợi đối với mỹ phẩm: Phụ lục số 18-MP.
1. Kể từ ngày Thông tư này có hiệu lực thi hành, tất cả các tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm mỹ phẩm ra thị trường Việt Nam phải thực hiện việc công bố sản phẩm mỹ phẩm theo quy định tại Thông tư này.
2. Đối với trường hợp các sản phẩm đã công bố từ ngày 10/3/2008 (theo quy định tại Quy chế Quản lý mỹ phẩm ban hành kèm theo Quyết định số 48/2007/QĐ-BYT ngày 31/12/2007 của Bộ trưởng Bộ Y tế) và được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm còn hiệu lực mà đáp ứng các quy định tại Thông tư này thì được phép tiếp tục sản xuất (đối với mỹ phẩm sản xuất trong nước), nhập khẩu (đối với mỹ phẩm nước ngoài) đến hết thời hạn của Phiếu công bố sản phẩm mỹ phẩm.
3. Những sản phẩm mỹ phẩm đưa ra lưu thông không đáp ứng yêu cầu về an toàn sản phẩm mỹ phẩm theo quy định tại Chương IV của Thông tư này, tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường phải thu hồi toàn bộ sản phẩm và thực hiện theo đúng quy định tại Thông tư này.
4. Các sản phẩm mỹ phẩm đã đưa ra lưu thông trong thời gian giấy phép còn hiệu lực, nếu đáp ứng yêu cầu về an toàn sản phẩm mỹ phẩm theo quy định tại Chương IV của Thông tư này thì được tiếp tục lưu thông trên thị trường đến hết hạn dùng của sản phẩm.
1. Thông tư này có hiệu lực thi hành kể từ ngày 01/4/2011.
2. Bãi bỏ Quyết định số 48/2007/QĐ-BYT ngày 31/12/2007 của Bộ trưởng Bộ Y tế về việc ban hành Quy chế quản lý mỹ phẩm, Quyết định số 40/2008/QĐ-BYT ngày 26/12/2008 của Bộ trưởng Bộ Y tế về việc phân cấp quản lý nhà nước về mỹ phẩm đối với mỹ phẩm sản xuất tại Việt Nam, Quyết định số 22/2008/QĐ-BYT ngày 02/7/2008 của Bộ trưởng Bộ Y tế về việc ủy quyền thực hiện chức năng quản lý mỹ phẩm cho Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài, tỉnh Tây Ninh tại Khu thương mại công nghiệp thuộc Khu kinh tế cửa khẩu Mộc Bài, tỉnh Tây Ninh, Quyết định số 3450/QĐ-BYT ngày 21/9/2010 của Bộ trưởng Bộ Y tế về việc ủy quyền thực hiện chức năng quản lý mỹ phẩm cho Ban Quản lý Khu kinh tế tỉnh Quảng Trị.
3. Thủ trưởng các đơn vị thuộc Bộ Y tế, các đơn vị trực thuộc Bộ Y tế; Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc trung ương và các tổ chức, cá nhân có liên quan chịu trách nhiệm thi hành Thông tư này.
4. Trong quá trình triển khai thực hiện, nếu có khó khăn, vướng mắc, các tổ chức, cá nhân gửi báo cáo về Bộ Y tế (Cục Quản lý dược, 138A Giảng Võ, Ba Đình, Hà Nội) để Bộ Y tế xem xét, giải quyết./.
|
|
KT. BỘ TRƯỞNG |
|
|
PHẦN DÀNH CHO CƠ QUAN QUẢN LÝ (FOR OFFICIAL USE) Ngày cấp số tiếp nhận (Date acknowledged): Số tiếp nhận Phiếu công bố (Product Notification No): Phiếu công bố có giá trị 05 năm kể từ ngày cấp.
|
PHIẾU CÔNG BỐ SẢN PHẨM MỸ PHẨM TEMPLATE FOR NOTIFICATION OF COSMETIC PRODUCT
þ Đánh dấu vào ô thích hợp (Tick where applicable)
THÔNG
TIN SẢN PHẨM
PARTICULARS OF PRODUCT
1. Tên nhãn hàng và tên sản phẩm (Name of brand & product):
1.1. Nhãn hàng (Brand)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1.2. Tên sản phẩm (Product Name)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1.3. Danh sách các dạng hoặc màu (List of Variants or Shade). Tên (Names)
_____________________________________________________________________________
_____________________________________________________________________________
2. Dạng sản phẩm (Product type(s))
□ Kem, nhũ tương, sữa,
gel hoặc dầu dùng trên da (tay, mặt, chân, ….)
Creams, emulsions, lotions, gels and oils for skin (hands, face, feet, etc)
□ Mặt nạ (chỉ trừ sản
phẩm làm bong da nguồn gốc hóa học)
Face masks (with the exception of chemical peeling products)
□ Chất phủ màu (lỏng,
nhão, bột)
Tinted bases (liquids, pastes, powders)
□ Phấn trang điểm, phấn
dùng sau khi tắm, bột vệ sinh,….
Make-up powders, after-bath powder, hygienic powders, etc.
□ Xà phòng rửa tay,
xà phòng khử mùi,…..
Toilet soaps, deodorant soaps, etc
□ Nước hoa, nước thơm
dùng vệ sinh,….
Perfumes, toilet waters and eau de Cologne
□ Sản phẩm để tắm (muối,
sữa, xà phòng, dầu, gel,….)
Bath or shower preparations (salts, lotions, foams, soaps, oils. gels, etc)
□ Sản phẩm tẩy lông
Depilatories
□ Sản phẩm khử mùi và chống mùi (giảm mùi mồ hôi)
Deodorants and anti-perspirants
□ Sản phẩm chăm sóc
tóc (Đề nghị đánh dấu vào dạng sản phẩm cụ thể bên dưới)
Hair care products (Please stick on specific product type below)
□ Nhuộm và tẩy màu
tóc
Hair tints and bleaches
□ Uốn tóc, duỗi tóc,
giữ nếp tóc
Products for waving, straightening and fixing
□ Các sản phẩm định dạng tóc
Setting products
□ Sản phẩm làm sạch (sữa, bột, dầu gội)
Cleansing products (lotions, powders, shampoos)
□ Sản phẩm dưỡng tóc
(sữa, kem, dầu)
Conditioning products (lotions, creams, oils)
□ Các sản phẩm tạo kiểu
tóc (sữa, keo xịt tóc, sáp)
Hairdressing products (lotions, lacquers, brilliantines)
□ Sản phẩm dùng cho cạo
râu hoặc sau khi cạo râu (kem, xà phòng, sữa,….)
Shaving product (creams, foams, lotions, etc)
□ Sản phẩm trang điểm
và tẩy trang dùng cho mặt và mắt
Products for making-up and removing make-up from the face and the eyes
□ Sản phẩm dùng cho
môi
Products intended for application to the lips
□ Sản phẩm chăm sóc
răng và miệng
Products for care of the teeth and the mouth
□ Sản phẩm dùng để
chăm sóc và trang điểm cho móng tay, móng chân
Products for nail care and make-up
□ Sản phẩm dùng để vệ
sinh cơ quan sinh dục ngoài
Products for external intimate hygiene
□ Sản phẩm chống nắng
Sunbathing products
□ Sản phẩm làm sạm da
mà không cần tắm nắng
Products for tanning without sun
□ Sản phẩm làm trắng
da
Skin whitening products
□ Sản phẩm chống nhăn
da
Anti-wrinkle products
□ Sản phẩm khác (đề
nghị ghi rõ)
Others (please specify)
3. Mục đích sử dụng (Intended use)
___________________________________________________________________________
___________________________________________________________________________
4. Dạng trình bày (Product presentation(s))
□ Dạng đơn lẻ (Single product)
□ Một nhóm các màu (Arange of colours)
□ Bảng các màu trong một dạng sản phẩm (Palette(s) in a range of one product type)
□ Các sản phẩm phối hợp trong một bộ sản phẩm (Combination products in a single kit)
□ Các dạng khác (đề nghị ghi rõ). Others (please specify)
THÔNG TIN VỀ CÔNG TY SẢN XUẤT/ĐÓNG GÓI/XUẤT KHẨU PARTICULARS OF MANUFACTURER(S)/ASSEMBLER(S)/EXPORTER
5. Tên công ty sản xuất (Name of manufacturer) (Liệt kê tất cả các công ty sản xuất, trong trường hợp nhiều công ty tham gia vào quá trình chế biến sản phẩm)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Địa chỉ công ty sản xuất (Nước sản xuất) (Address of manufacturer (state country)):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Country |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Tel: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fax: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6. Tên công ty đóng gói (Đề nghị đánh dấu vào mục thích hợp. Có thể đánh dấu nhiều hơn 01 ô) (Name of assembler (Please tick accordingly. May tick more than one box)):
□ Đóng gói chính □ Đóng gói thứ cấp
Primary assembler Secondary assembler
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Địa chỉ của công ty đóng gói(Address of assembler (state country)):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Country |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Tel: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fax: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7. Tên nước xuất khẩu (Đề nghị đánh dấu vào mục thích hợp. Chỉ áp dụng đối với sản phẩm mỹ phẩm nhập khẩu) (Name of exporting country (Please tick accordingly. Only apply to imported cosmetic products)):
|
Country |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Sản phẩm mỹ phẩm được lưu hành tự do tại (Cosmetic product(s) are free sold in):
- Nước xuất khẩu (Exporting country): □
- Nước sản xuất (Manufacturing country): □
THÔNG TIN VỀ TỔ CHỨC, CÁ NHÂN CHỊU TRÁCH NHIỆM ĐƯA SẢN PHẨM MỸ PHẨM RA THỊ TRƯỜNG
PARTICULARS OF LOCAL COMPANY RESPONSIBLE FOR PLACING THE COSMETIC PRODUCT IN THE MARKET
8. Tên công ty (Name of company):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Địa chỉ công ty (Address of company):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tel: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fax: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Số giấy phép kinh doanh/Số giấy phép hoạt động
Business Registration Number/License to Operate Number
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
THÔNG TIN VỀ NGƯỜI ĐẠI DIỆN THEO PHÁP LUẬT CỦA CÔNG TY PARTICULARS OF PERSON REPRESENTING THE LOCAL COMPANY
9. Họ và tên (Name of person):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tel: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Email: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Chức vụ ở công ty (Designation in the company):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
THÔNG
TIN VỀ CÔNG TY NHẬP KHẨU
PARTICULARS OF IMPORTER
10.Tên công ty nhập khẩu (Name of importer):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Địa chỉ công ty nhập khẩu (Address of importer):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Tel: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fax: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
DANH
SÁCH THÀNH PHẦN
PRODUCT INGREDIENT LIST
11. Đề nghị kiểm tra ô sau đây (Please check the following boxes):
□ Tôi đã kiểm tra bản sửa đổi từ Phụ lục II đến Phụ lục VII của danh mục các thành phần mỹ phẩm ASEAN như được công bố trên bản sửa đổi gần đây nhất của Hiệp định mỹ phẩm ASEAN. Tôi xin xác nhận rằng sản phẩm được đề cập đến trong bản công bố này không chứa bất cứ một thành phần bị cấm nào và cũng tuân thủ với danh mục hạn chế và các điều kiện quy định trong các phụ lục.
I have examined the latest revisions of the Annexes II to VII of the ASEAN Cosmetic Ingredient Listing as published in the latest amendment of the ASEAN Cosmetic Directive and confirmed that the product in this notification does not contain any prohibited substances and is in compliance with the restrictions and conditions stipulated in the Annexes.
□ Tôi đảm nhận trách nhiệm trả lời và hợp tác toàn diện với cơ quan có thẩm quyền về bất kỳ hoạt động kiểm soát sau khi bán hàng khi có yêu cầu bởi cơ quan có thẩm quyền.
I undertake to respond to and cooperate fully with the regulatory authority with regard to any subsequent post-marketing activity initiated by the authority.
Danh sách thành phần đầy đủ (Product full ingredient list)
(Yêu cầu ghi đầy đủ danh sách tất cả các thành phần và tỉ lệ % của những chất có giới hạn về nồng độ, hàm lượng sử dụng trong mỹ phẩm - To submit ingredient list with percentages of restricted ingredients)
|
No |
Tên đầy đủ thành phần (tên danh pháp quốc tế hoặc tên khoa học chuẩn đã được công nhận) Full Ingredient name (use INCI or approved nomenclature in standard references) |
Tỉ lệ % của các chất có giới hạn về nồng độ, hàm lượng (Percentage of restricted ingredients) |
Ghi chú |
|
1 |
|
|
|
|
2 |
|
|
|
|
3 |
|
|
|
|
4 |
|
|
|
|
5 |
|
|
|
|
6 |
|
|
|
|
7 |
|
|
|
|
8 |
|
|
|
|
9 |
|
|
|
|
... |
|
|
|
CAM KẾT (DECLARATION)
1. Thay mặt cho công ty, tôi xin cam kết sản phẩm được đề cập trong Phiếu công bố này đạt được tất cả các yêu cầu của Hiệp định mỹ phẩm ASEAN và các phụ lục kèm theo.
I hereby declare on behalf of my company that the product in the notification meets all the requirements of the ASEAN Cosmetic Directive, its Annexes and Appendices.
2. Tôi xin chịu trách nhiệm tuân thủ các điều khoản sau đây (I undertake to abide by the following conditions):
i. Đảm bảo có sẵn để cung cấp các thông tin kỹ thuật và tính an toàn khi cơ quan có thẩm quyền yêu cầu và có đầy đủ hồ sơ về các sản phẩm đã được phân phối để báo cáo trong trường hợp sản phẩm phải thu hồi.
Ensure that the product’s technical and safety information is made readily available to the regulatory authority concerned (“the Authority”) and to keep records of the distribution of the products for product recall purposes;
ii. Phải thông báo ngay cho cơ quan có thẩm quyền về các tác dụng phụ nghiêm trọng1 của sản phẩm gây chết người hoặc đe dọa tính mạng bằng điện thoại, fax, thư điện tử hoặc văn bản trong thời hạn 07 ngày kể từ ngày biết thông tin.
Notify the Authority of fatal or life threatening serious adverse event1 as soon as possible by telephone, facsimile transmission, email or in writing, and in any case, no later than 7 calendar days after first knowledge;
iii. Phải hoàn thành báo cáo tác dụng phụ của sản phẩm (theo mẫu quy định)2 trong thời hạn 08 ngày làm việc kể từ ngày thông báo cho cơ quan có thẩm quyền về những tác dụng phụ nghiêm trọng như đã nêu trong mục 2 ii nói trên và cung cấp bất cứ thông tin nào theo yêu cầu của cơ quan có thẩm quyền.
Complete the Adverse Cosmetic Event Report Form2 within 8 calendar days from the date of my notification to the Authority in para 2 ii. above, and to provide any other information as may be requested by the Authority;
iv. Thông báo ngay cho cơ quan có thẩm quyền về các tác dụng phụ nghiêm trọng nhưng không gây chết người hoặc đe dọa đến tính mạng của sản phẩm và trong bất cứ trường hợp nào, việc báo cáo (sử dụng mẫu báo cáo) về tác dụng phụ phải được tiến hành trong thời hạn 15 ngày kể từ ngày biết về tác dụng phụ này.
Report to the Authority of all other serious adverse events that are not fatal or life threatening as soon as possible, and in any case, no later than 15 calendar days after first knowledge, using the Adverse Cosmetic Event Report Form;
v. Công bố với cơ quan có thẩm quyền khi có bất cứ sự thay đổi nào trong bản công bố này.
Notify the Authority of any change in the particulars submitted in this notification;
3. Tôi xin cam đoan rằng những thông tin được đưa ra trong bản công bố này là đúng sự thật. Tất cả các tài liệu, các thông tin liên quan đến nội dung công bố sẽ được cung cấp và các tài liệu đính kèm là bản hợp pháp hoặc sao y bản chính.
I declare that the particulars given in this notification are true, all data, and information of relevance in relation to the notification have been supplied and that the documents enclosed are authentic or true copies.
4. Tôi hiểu rằng tôi sẽ có trách nhiệm để đảm bảo tất cả các lô sản phẩm của chúng tôi đều đáp ứng các yêu cầu pháp luật, và tuân thủ tất cả tiêu chuẩn và chỉ tiêu sản phẩm đã được công bố với cơ quan có thẩm quyền.
I understand that I shall be responsible for ensuring that each consignment of my product continues to meet all the legal requirements, and conforms to all the standards and specifications of the product that I have declared to the Authority.
5. Tôi hiểu rằng trong trường hợp có tranh chấp pháp luật, tôi không được quyền sử dụng bản công bố sản phẩm mỹ phẩm đã được cơ quan có thẩm quyền chấp nhận nếu sản phẩm của chúng tôi không đạt được các yêu cầu về tiêu chuẩn, chỉ tiêu mà chúng tôi đã công bố.
I understand that I cannot place reliance on the acceptance of my product notification by the authority in any legal proceedings concerning my product, in the event that my product has failed to conform to any of the standards or specifications that I had previously declared to the Authority.
___________________________________________________________________
Tên và
chữ ký của người đại diện theo pháp luật của công ty
[Name and Signature of person representing the local company]
|
_____________ Dấu của
công ty |
_____________ Ngày [Date] |
TÀI LIỆU HƯỚNG DẪN VỀ CÔNG BỐ SẢN
PHẨM MỸ PHẨM
GUIDANCE DOCUMENT ON PRODUCT NOTIFICATION
1. Tên nhãn hàng và tên sản phẩm. Name of brand and product
Tên đầy đủ của sản phẩm phải được cung cấp, theo trình tự sau: tên nhãn hàng, dòng sản phẩm (nếu có), tên sản phẩm. Nếu là một màu riêng lẻ được công bố thì ghi tên màu và số màu (ví dụ: L’oreal Feria Color 3D Hot Ginger). Nếu có nhiều màu thì tên và số màu của mỗi màu phải được công bố.
The complete name of the product should be given, in the following sequence: brand name, line name (if applicable), product name, if a single shade is notified, the shade name/number (e.g. L’oreal Feria Color 3D Hot Ginger). If there are different shades, the shade name/number for each shade shall be declared.
2. Dạng sản phẩm. Product types
Danh sách minh họa là chưa đầy đủ và có thể đề cập đến các dạng sản phẩm khác không có trong danh sách bằng cách lựa chọn mục “các dạng khác” và ghi rõ dạng sản phẩm. Có thể lựa chọn nhiều hơn một dạng sản phẩm, ví dụ “ bath hoặc shower” và “ sản phẩm chăm sóc tóc” nếu như sản phẩm sử dụng được trong các trường hợp này.
The illustrative list is not exhaustive and you can include other types of cosmetic products not in the list by selecting others and specifying what it is. More than one category can be selected, e.g. ‘Bath or shower preparations’ and ‘Hair-care products’ can be selected if your product is both a shower gel and hair shampoo.
3. Mục đích sử dụng. Intended use
Là thông tin về chức năng hoặc công dụng của sản phẩm, không phải cách sử dụng, ví dụ giữ ẩm cho da mặt, da tay,...
This refers to the function or use of the product and not the directions for use e.g. to moisturize the face, hand, etc.
4. Dạng trình bày. Product presentation(s)
Chỉ lựa chọn một dạng thích hợp nhất trong 4 dạng sản phẩm. Sau đây là giải thích về các dạng sản phẩm.
Please select only one out of the 4 choices that best fit the presentation type of the product. The following is an explanation of the presentation types:
- “Dạng đơn lẻ” được trình bày trong một dạng đóng gói đơn lẻ.
“A single product” exists in a single presentation form.
- “Một nhóm các màu” là một nhóm các sản phẩm mỹ phẩm có thành phần tương tự nhau và được sản xuất bởi cùng một nhà sản xuất, có cùng mục đích sử dụng, nhưng có màu sắc khác nhau (ví dụ như son, màu mắt, hoặc đánh móng tay) nhưng không phải là dạng đóng gói kết hợp của các dạng sản phẩm khác nhau.
"A range of colours” is a range of cosmetic products, which are similar in composition and produced by the same manufacturer, and are intended for the same use but are available in different shades of colour (e.g. lipsticks, eye shadows or nail polish but not composite packs of different types).
- “Bảng các màu trong một dạng sản phẩm” là một nhóm các màu như được định nghĩa ở trên, được đóng trong một loạt các bảng.
"Palette(s) in a range of one product type” refers to arange of colours as defined above, which may be presented in a series of palettes.
- “Các sản phẩm phối hợp trong một bộ sản phẩm” là các dạng sản phẩm giống hoặc khác nhau và được bán trong cùng một bao gói. Không thể bán riêng từng loại (ví dụ như một hộp các màu mắt và môi, một hộp chứa cả các dạng kem chăm sóc da).
"Combination products in a single kit” refer to similar and/ or different product types packed and sold in a single kit. They cannot be sold separately (e.g. a make-up kit of eye and lip colours; a set of skin-care products sold in a single kit).
5. Thông tin về nhà sản xuất/ đóng gói. Particulars of the manufacturer(s)/ Assembler(s)
Có thể có trên một công ty sản xuất hoặc đóng gói cho một sản phẩm (là các công ty tham gia các công đoạn sản xuất để sản xuất ra một sản phẩm hoàn chỉnh). Phải nêu rõ tên và địa chỉ đầy đủ của từng công ty (trường hợp địa chỉ trụ sở chính khác địa chỉ cơ sở sản xuất thì phải khai báo cả hai).
There may be more than one manufacturer and/or assembler for one product. The full names and contact details of each of them must be submitted (If the address of main office and factory of the manufacturer are different, it is required to notify both of them).
- Công ty sản xuất là công ty tham gia vào bất kỳ giai đoạn nào của quá trình tạo ra sản phẩm mỹ phẩm. Quá trình sản xuất bao gồm tất cả các giai đoạn từ sản xuất bán thành phẩm và thành phẩm, xây dựng công thức và sản xuất (ví dụ như nghiền, trộn, gói và hoặc đóng gói), kiểm tra chất lượng, xuất xưởng và các quá trình kiểm soát liên quan.
Amanufacturer is a company which is engaged in any process carried out in the course of making the cosmetic product. The manufacturing process includes all operations of bulk intermediates and products, formulation and production (such as grinding, mixing, encapsulation and/ or packaging), quality control, release and the related controls.
- Công ty đóng gói chính là công ty tham gia vào qúa trình đóng gói sản phẩm vào bao bì đóng gói chính/ trực tiếp, bao bì này được hoặc sẽ được dán nhãn trước khi sản phẩm được bán hoặc phân phối.
A primary assembler is a company which is engaged in a process of enclosing the product in a primary/ immediate container which is labelled or to be labelled before the product is sold or supplied in it.
- Công ty đóng gói thứ cấp là công ty chỉ tham gia vào quá trình dán nhãn cho bao gói mà sản phẩm đã được đóng vào trong bao gói chính, hoặc đóng bao gói chính vào trong hộp carton, sau đó dán nhãn, trước khi bán hoặc phân phối.
A secondary assembler is a company which is engaged only in a process of labelling the product container where the product is already enclosed in its primary container and/ or packing the product which is already enclosed in its labelled primary container into a carton which is labelled or to be labelled, before the product is sold or supplied.
6. Thông tin về tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường. Particulars of company
Đó là tổ chức, cá nhân chịu trách nhiệm đưasản phẩm ra thị trường, có thể là công ty sản xuất trong nước hoặc đại lý được ủy quyền bởi nhà sản xuất để bán sản phẩm ra thị trường hoặc đó, là công ty chịu trách nhiệm bán sản phẩm trên thị t rường Việt Nam. Số Giấy chứng nhận đăng ký kinh doanh hoặc giấy phép tương đương phải được nêu rõ trong mẫu công bố, nếu có.
It refers to the local company responsible for placing the cosmetic products in the market, which may be a local manufacturer or an agent appointed by a manufacturer to market the product or the company that is responsible for bringing in the product for sale in Viet Nam, etc. The business registration number or its equivalent should be indicated in the notification form, if applicable.
7. Thông tin về người đại diện theo pháp luật cho công ty. Particulars of the person representing the local company
Người đại diện cho công ty để nộp hồ sơ công bố phải có đủ trình độ và kinh nghiệm theo quy định của luật pháp và luật hành nghề của các nước thành viên, là người đại diện theo pháp luật của công ty nêu trên Giấy chứng nhận đăng ký kinh doanh
The person who represents the company to submit the product notification must possess adequate knowledge or experience in accordance with the legislation and practice of the Member Country.
8. Thành phần đầy đủ và danh pháp. Full ingredient listing and nomenclature
a) Tất cả các thành phần của mỹ phẩm phải được xác định bằng danh pháp trong ấn phẩm mới nhất về danh pháp chuẩn (International Cosmetic Ingredient Dictionary, British Pharmacopoeia, United States Pharmacopoeia, Chemical Abstract Services, Japanese Standard Cosmetic Ingredient, Japanese Cosmetic Ingredients Codex). Tên thực vật và dịch chiết từ thực vật phải được xác định bằng chi, loài. Tên chi thực vật có thể rút ngắn. Các thành phần có nguồn gốc từ động vật cần nêu chính xác tên khoa học của loài động vật đó. Các thành phần sau đây không được coi là thành phần của sản phẩm:
All the ingredients in the product must be specified by using the nomenclature from the latest edition of standard references (Refer to appendix A). Botanicals and extract of botanicals should be identified by its genus and species. The genus may be abbreviated. If ingredients derived from animals, it is required to specify the scientific name of the animals. The following are not regarded as ingredients:
- Tạp chất trong nguyên liệu được sử dụng.
Impurities in the raw materials used;
- Các nguyên liệu được sử dụng vì mục đích kỹ thuật nhưng không có mặt trong sản phẩm thành phẩm.
Subsidiary technical materials used in the preparation but not present in the final product;
- Các hoá chất được sử dụng với một số lượng cần thiết được kiểm soát chặt chẽ như dung môi hoặc chất giữ mùi hoặc các thành phần tạo mùi. Các thành phần nước hoa và chất tạo hương và các nguyên liệu của chúng có thể viết dưới dạng “hương liệu” (perfume, fragrance).
Materials used in strictly necessary quantities as solvents, or as carriers for perfume and aromatic compositions.
Nồng độ của các thành phần phải được công bố nếu như đó là các thành phần nằm trong danh mục hạn chế sử dụng được xác định trong các phụ lục của Hướng dẫn về mỹ phẩm ASEAN.
The percentage of ingredients must be declared if they are substances with restrictions for use as specified in the annexes of the ASEAN Cosmetic Directive.
b) Đối với sản phẩm chứa một nhóm các màu hoặc các sản phẩm trong cùng một bao gói, công bố thành phần đầy đủ theo dạng sau:
For a range of colours/shades or products in a single kit, complete the Product Ingredient List in the following format:
- Danh sách thành phần của dạng cơ bản
List ingredients in the Base Formulation
- “Có thể chứa” và danh sách các màu
‘May contain’ and list each colour/shade
c) Với dạng phối hợp các sản phẩm khác nhau trong cùng một đóng gói, liệt kê mỗi sản phẩm và công thức tương ứng cho từng sản phẩm. Có thể mở rộng mẫu công bố nếu cần thêm khoảng trống để điền thông tin.
For combination products in a kit, list each product and its corresponding formulation individually. You can extend the form when more space is needed.
HƯỚNG DẪN CỦA ASEAN
VỀ CÔNG BỐ TÍNH NĂNG CỦA SẢN PHẨM MỸ PHẨM
Việc đánh giá công bố tính năng sản phẩm (Product claim) không thể tách rời với việc xem xét liệu một sản phẩm có phải là sản phẩm mỹ phẩm hay không. Việc quyết định sản phẩm có phải là mỹ phẩm hay không phải dựa trên một số yếu tố, trong đó, tính năng sản phẩm (gọi tắt là Claim) là một trong những yếu tố quan trọng. Bản hướng dẫn một quy trình đơn giản gồm 5 bước quyết định để xác định sản phẩm và công bố tính năng có phù hợp cho một sản phẩm mỹ phẩm không.
Bản hướng dẫn cũng đưa ra một số ví dụ về công bố tính năng không được chấp nhận cho mỹ phẩm. Tuy nhiên, danh sách này không được xem là một danh sách đầy đủ, quyết định cuối cùng vẫn là của cơ quan quản lý.
Quy trình quyết định sản phẩm là mỹ phẩm và công bố tính năng sản phẩm mỹ phẩm được phép (xem biểu đồ tóm tắt)
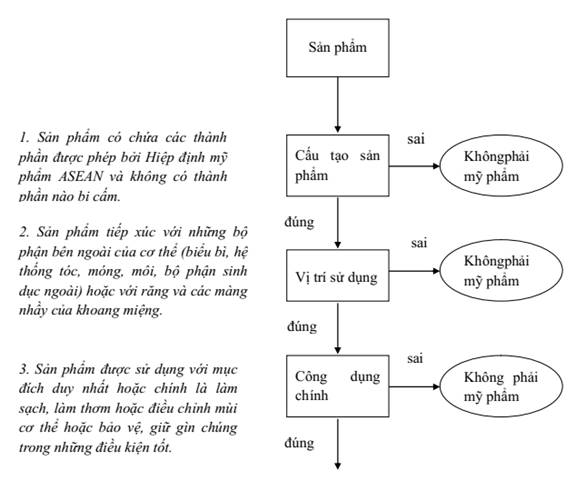
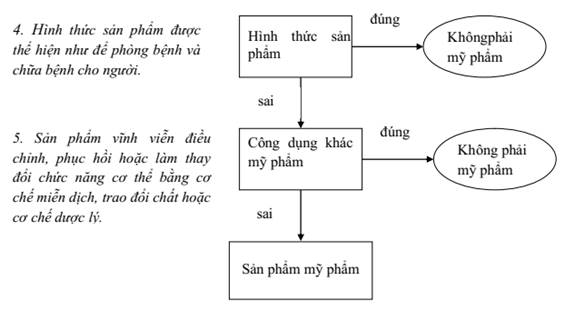
Trong đó:
- Thành phần cấu tạo sản phẩm mỹ phẩm
Sản phẩm chỉ chứa những thành phần tuân thủ theo các Phụ lục của Hiệp định mỹ phẩm ASEAN và không chứa bất cứ thành phần nào nằm trong Phụ lục các chất cấm sử dụng trong mỹ phẩm với điều kiện đi kèm của Hiệp định mỹ phẩm ASEAN.
- Vị trí sử dụng của sản phẩm mỹ phẩm
Mỹ phẩm chỉ tiếp xúc bên ngoài với những phần khác nhau của cơ thể (biểu bì, hệ thống tóc, móng, môi và cơ quan sinh dục ngoài) hoặc với răng và các màng nhầy của khoang miệng.
Sản phẩm dùng để uống, tiêm, hoặc tiếp xúc với những phần khác của cơ thể ví dụ như màng nhầy của đường mũi hoặc bộ phận sinh dục trong không được xem là mỹ phẩm.
- Công dụng chính của sản phẩm mỹ phẩm
Mỹ phẩm được sử dụng cho những phần cho phép của cơ thể với mục đích duy nhất hoặc mục đích chính là làm sạch, làm thơm hoặc thay đổi vẻ bề ngoài hoặc điều chỉnh mùi cơ thể hoặc bảo vệ, giữ gìn chúng trong điều kiện tốt.
(Lưu ý sản phẩm có thể có công dụng thứ hai hoặc công dụng phụ nằm ngoài phạm vi nói trên).
- Cách thể hiện của sản phẩm mỹ phẩm
Sản phẩm mỹ phẩm không được thể hiện như một sản phẩm để chữa bệnh hoặc phòng bệnh cho người. Những đặc điểm sau cần phải được xem xét kỹ:
I. Lời giới thiệu tính năng, quảng cáo sản phẩm và ngữ cảnh.
II. Bao bì/ nội dung nhãn và nhãn bổ sung (bao gồm cả hình ảnh minh họa).
III. Tài liệu khuyến mãi bao gồm giấy chứng nhận hoặc tài liệu do các bên gia công ban hành thay cho nhà cung cấp.
IV. Các hình thức quảng cáo.
V. Hình thức sản phẩm và cách nó được sử dụng, ví dụ như: viên con nhộng, thuốc viên, dạng tiêm,...
VI. Mục tiêu cá biệt của các thông tin quảng cáo, ví dụ: một nhóm người nhất định với/hoặc có những tổn thương đặt biệt đối với những bệnh tật/ các phản ứng có hại.
- Những ảnh hưởng sinh lý học của sản phẩm
Tất cả các sản phẩm có ảnh hưởng đến chức năng của cơ thể đều có ảnh hưởng đến quá trình trao đổi chất. Đặc tính của mỹ phẩm là tạo nên các ảnh hưởng/ hiệu quả không vĩnh viễn và cần phải sử dụng thường xuyên để duy trì hiệu quả.
Điều cần lưu ý đầu tiên là tất cả những tính năng phù hợp dùng cho các loại sản phẩm như trong danh mục các sản phẩm mỹ phẩm (Phụ lục I của Hiệp định mỹ phẩm ASEAN) hiển nhiên được xem là mỹ phẩm.
Một số ví dụ về các tính năng thường gặp không được chấp nhận đối với mỹ phẩm theo từng loại sản phẩm (đây chưa phải là danh mục đầy đủ):
|
Loại Sản Phẩm |
Câu giới thiệu tính năng sản phẩm không được chấp nhận |
|
Chăm sóc tóc |
• Loại bỏ gàu vĩnh viễn • Phục hồi tế bào tóc / nang tóc • Làm dày sợi tóc • Chống rụng tóc • Kích thích mọc tóc |
|
Sản phẩm làm rụng lông |
• Ngăn ngừa/ dừng sự phát triển của lông |
|
Sản phẩm dùng cho móng |
• Đề cập đến việc nuôi dưỡng làm ảnh hưởng đến sự phát triển móng |
|
Sản phẩm chăm sóc da |
• Ngăn chặn, làm giảm hoặc làm đảo ngược những thay đổi sinh lý và sự thoái hoá do tuổi tác • Xóa sẹo • Tác dụng tê • Trị mụn, chữa khỏi, làm lành mụn • Chữa viêm da • Giảm kích thước cơ thể • Săn chắc cơ thể/ săn chắc ngực • Giảm/ kiểm soát sự sưng tấy phù nề • Loại bỏ/ giảm mỡ/ giảm béo • Diệt nấm • Diệt virus • Giảm dị ứng |
|
Sản phẩm vệ sinh và chăm sóc răng miệng |
• Chữa trị hay phòng chống các bệnh áp-xe răng, song nướu, viêm lợi, loét miệng, nha chu, chảy mủ quanh răng, viêm vòm miệng, răng bị xô lệch, bệnh về nhiễm trùng răng miệng,... • Làm trắng lại các vết ố do Tetracyline |
|
Sản phẩm ngăn mùi |
• Dừng quá trình ra mồ hôi |
|
Nước hoa/ Chất thơm |
• Tăng cường cảm xúc • Hấp dẫn giới tính |
Những tính năng trên có thể được làm giảm nhẹ đi và mang tính mỹ phẩm hơn. Ví dụ: đối với tính năng “loại bỏ hoàn toàn dầu cho da” có thể điều chỉnh làm nhẹ hơn như sau:
• Giúp loại bỏ dầu cho da • Giảm bóng cho da dầu
• Phù hợp đối với loại da dầu • Làm cho da bạn cảm thấy bớt dầu
Viết tắt tên các tỉnh, thành phố trực thuộc Trung ương và một số Ban quản lý Khu kinh tế
|
STT |
Tên tỉnh, thành phố |
Ký hiệu |
STT |
Tên tỉnh, thành phố |
Ký hiệu |
|
1 |
An Giang |
AG |
34 |
Lai Châu |
LC |
|
2 |
Bắc Cạn |
BC |
35 |
Lâm Đồng |
LĐ |
|
3 |
Bình Dương |
BD |
36 |
Lạng Sơn |
LS |
|
4 |
Bình Định |
BĐ |
37 |
Lào Cai |
LCa |
|
5 |
Bắc Giang |
BG |
38 |
Long An |
LA |
|
6 |
Bạc Liêu |
BL |
39 |
Nam Định |
NĐ |
|
7 |
Bắc Ninh |
BN |
40 |
Nghệ An |
NA |
|
8 |
Bình Phước |
BP |
41 |
Ninh Bình |
NB |
|
9 |
Bến Tre |
BT |
42 |
Ninh Thuận |
NT |
|
10 |
Bình Thuận |
BTh |
43 |
Phú Thọ |
PT |
|
11 |
Bà Rịa - Vũng Tàu |
BV |
44 |
Phú Yên |
PY |
|
12 |
Cao Bằng |
CB |
45 |
Quảng Bình |
QB |
|
13 |
Cà Mau |
CM |
46 |
Quảng Nam |
QNa |
|
14 |
Cần Thơ |
CT |
47 |
Quảng Ngãi |
QNg |
|
15 |
Đà Nẵng |
ĐNa |
48 |
Quảng Ninh |
QN |
|
16 |
Đắc Lắc |
ĐL |
49 |
Quảng Trị |
QT |
|
17 |
Đắc Nông |
ĐNô |
50 |
Tp. Hồ Chí Minh |
HCM |
|
18 |
Điện Biên |
ĐB |
51 |
Sơn La |
SL |
|
19 |
Đồng Nai |
ĐN |
52 |
Sóc Trăng |
ST |
|
20 |
Đồng Tháp |
ĐT |
53 |
Tây Ninh |
TN |
|
21 |
Gia Lai |
GL |
54 |
Thái Bình |
TB |
|
22 |
Hà Giang |
HG |
55 |
Thái Nguyên |
TNg |
|
23 |
Hà Nam |
HNa |
56 |
Thanh Hoá |
TH |
|
24 |
Hà Nội |
HN |
57 |
Thừa Thiên Huế |
TTH |
|
25 |
Hà Tĩnh |
HT |
58 |
Tiền Giang |
TG |
|
26 |
Hải Dương |
HD |
59 |
Tuyên Quang |
TQ |
|
27 |
Hải Phòng |
HP |
60 |
Trà Vinh |
TV |
|
28 |
Hậu Giang |
HGi |
61 |
Vĩnh Long |
VL |
|
29 |
Hòa Bình |
HB |
62 |
Vĩnh Phúc |
VP |
|
30 |
Hưng Yên |
HY |
63 |
Yên Bái |
YB |
|
31 |
Kiên Giang |
KG |
64 |
Ban Quản lý Khu kinh tế cửa khẩu Mộc Bài - tỉnh Tây Ninh |
BQLMB |
|
32 |
Khánh Hoà |
KH |
65 |
Ban Quản lý Khu kinh tế tỉnh Quảng Trị |
BQLQT |
|
33 |
Kon Tum |
KT |
|
|
|
THAY ĐỔI SAU KHI CÔNG BỐ SẢN PHẨM MỸ PHẨM
Tùy thuộc vào nội dung thay đổi, quy định như sau:
|
Nội dung thay đổi |
Công bố sản phẩm |
|
Thay đổi nhãn hàng |
Công bố mới |
|
Thay đổi tên sản phẩm |
Công bố mới |
|
Thay đổi công ty chịu trách nhiệm đưa sản phẩm ra thị trường |
Công bố mới |
|
Thay đổi dạng sản phẩm |
Công bố mới |
|
Thay đổi mục đích sử dụng |
Công bố mới |
|
Thay đổi công thức |
Công bố mới |
|
Thay đổi nhà sản xuất hoặc đóng gói (tên và/hoặc địa chỉ) |
Công bố mới |
|
Thay đổi dạng trình bày của sản phẩm |
Bổ sung |
|
Tên và/hoặc địa chỉ của công ty chịu trách nhiệm đưa sản phẩm ra thị trường nhưng không thay đổi số Giấy chứng nhận đăng ký kinh doanh hoặc Giấy chứng nhận đầu tư. |
Bổ sung |
|
Tên và/ hoặc địa chỉ của công ty nhập khẩu |
Bổ sung |
|
Thay đổi người đại diện cho công ty |
Bổ sung |
|
Thay đổi kích cỡ bao gói, chất liệu bao bì, nhãn sản phẩm |
Bổ sung, nhưng không áp dụng nếu như thông tin cần thiết không được đề cập đến trong Phiếu công bố. |
QUY ĐỊNH CỦA ASEAN VỀ GIỚI HẠN KIM LOẠI NẶNG VÀ VI SINH VẬT TRONG SẢN PHẨM MỸ PHẨM
1. Giới hạn kim loại nặng (ACM THA 05 Testing Method):
|
STT |
Chỉ tiêu |
Giới hạn |
|
1 |
Thủy ngân |
Nồng độ tối đa cho phép có trong sản phẩm mỹ phẩm là 1 phần triệu (1 ppm) |
|
2 |
Asen |
Nồng độ tối đa cho phép có trong sản phẩm mỹ phẩm là 5 phần triệu (5 ppm) |
|
3 |
Chì |
Nồng độ tối đa cho phép có trong sản phẩm mỹ phẩm là 20 phần triệu (20 ppm) |
2. Giới hạn vi sinh vật (ACM THA 06 Testing Method):
|
STT |
Chỉ tiêu |
Giới hạn |
|
|
Sản phẩm dành cho trẻ em dưới 03 tuổi, sản phẩm tiếp xúc với vùng mắt hoặc niêm mạc |
Sản phẩm khác |
||
|
1 |
Tổng số vi sinh vật đếm được |
=<500 cfu/g |
=<1000 cfu/g |
|
2 |
P. aeruginosa |
Không được có trong 0,1g hoặc 0,1 ml mẫu thử |
Không được có trong 0,1g hoặc 0,1ml mẫu thử |
|
3 |
S. aureus |
Không được có trong 0,1g hoặc 0,1 ml mẫu thử |
Không được có trong 0,1g hoặc 0,1ml mẫu thử |
|
4 |
C. albicans |
Không được có trong 0,1g hoặc 0,1 ml mẫu thử |
Không được có trong 0,1g hoặc 0,1ml mẫu thử |
HỒ SƠ THÔNG TIN SẢN PHẨM
(PIF - Product Information File)
Hồ sơ thông tin sản phẩm bao gồm các nội dung sau:
Phần 1. Tài liệu hành chính và tóm tắt về sản phẩm
- Tài liệu hành chính:
+ Bản sao Phiếu công bố sản phẩm mỹ phẩm có số tiếp nhận của cơ quan quản lý nhà nước có thẩm quyền (Đối với mỹ phẩm nước ngoài và mỹ phẩm sản xuất trong nước công bố kể từ ngày 10/3/2008); Phiếu tiếp nhận Bản công bố tiêu chuẩn chất lượng mỹ phẩm (Đối với mỹ phẩm sản xuất trong nước được cấp phiếu tiếp nhận trước ngày 10/3/2008); Giấy phép lưu hành mỹ phẩm (Đối với mỹ phẩm nước ngoài được cấp số đăng ký lưu hành trước ngày 10/3/2008);
+ Giấy ủy quyền của nhà sản xuất hoặc chủ sở hữu sản phẩm hoặc thư thoả thuận liên quan đến sản phẩm;
+ Giấy chứng nhận lưu hành tự do - CFS (đối với mỹ phẩm nước ngoài nhập khẩu);
+ Các tài liệu hành chính có liên quan khác (Giấy chứng nhận đăng ký kinh doanh hoặc Giấy phép đầu tư của tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường);
+ Các thành phần và tỷ lệ phần trăm của tất cả các thành phần trong công thức.
- Nhãn và thông tin sản phẩm:
+ Nhãn sản phẩm;
+ Tờ hướng dẫn sử dụng (nếu có).
- Công bố về sản xuất:
+ Công bố của nhà sản xuất về việc sản phẩm được sản xuất phù hợp với các nguyên tắc, tiêu chuẩn “Thực hành tốt sản xuất mỹ phẩm” của Hiệp hội các nước Đông Nam Á (CGMP-ASEAN) hoặc tương đương;
+ Hệ thống ghi số lô/ mã sản phẩm.
- Đánh giá an toàn sản phẩm mỹ phẩm:Công bố an toàn (với ý kiến kết luận có chữ ký, tên và văn bằng chứng chỉ của đánh giá viên).
- Tóm tắt những tác dụng không mong muốn trên người (nếu có).
- Tài liệu thuyết minh tính năng, công dụng của sản phẩm mỹ phẩm (tóm tắt): Báo cáo về đánh giá tính năng, công dụng của sản phẩm dựa theo thành phần và kết quả thử nghiệm.
Phần 2. Chất lượng của nguyên liệu
- Tiêu chuẩn chất lượng và phương pháp kiểm nghiệm của nguyên liệu. Đối với thành phần hương liệu, nêu rõ tên và mã số hương liệu, tên và địa chỉ nhà cung cấp, cam kết phù hợp với hướng dẫn của Hiệp hội Hương liệu Quốc tế (IFRA).
- Dữ liệu an toàn của nguyên liệu dựa trên thông tin từ nhà cung cấp, những dữ liệu đã được công bố hoặc báo cáo từ các Uỷ ban khoa học (ACSB, SCCP, CIR).
Phần 3. Chất lượng của thành phẩm
- Công thức của sản phẩm: Ghi tên đầy đủ các thành phần theo danh pháp quốc tế và tỷ lệ phần trăm của các thành phần trong công thức. Nêu rõ công dụng của từng thành phần nguyên liệu;
- Sản xuất:
+ Thông tin chi tiết về nhà sản xuất: quốc gia, tên và địa chỉ nhà sản xuất, nhà đóng gói;
+ Tóm tắt quy trình sản xuất;
+ Các thông tin chi tiết thêm về quy trình sản xuất, quản lý chất lượng và các hồ sơ liên quan về sản xuất, cần được chuẩn bị sẵn sàng tuỳ theo yêu cầu cơ quan quản lý.
- Tiêu chuẩn và các phương pháp thử của thành phẩm:
+ Các chỉ tiêu sử dụng kiểm tra giới hạn vi sinh trong thành phẩm;
+ Các phương pháp thử tương ứng với tiêu chuẩn chất lượng để kiểm tra mức độ đạt;
- Báo cáo tóm tắt về độ ổn định của sản phẩm (cho sản phẩm có tuổi thọ dưới 30 tháng): Báo cáo và dữ liệu nghiên cứu độ ổn định hoặc đánh giá độ ổn định để thuyết minh cho hạn sử dụng của sản phẩm.
Phần 4. An toàn và hiệu quả
- Đánh giá tính an toàn: Báo cáo đánh giá về tính an toàn trên người của thành phẩm dựa theo thành phần trong công thức, cấu trúc hoá học của thành phần và ngưỡng gây hại (có tên và chữ ký của đánh giá viên);
- Sơ yếu lý lịch của đánh giá viên về tính an toàn của sản phẩm;
- Báo cáo mới nhất về tác dụng phụ hay tác dụng không mong muốn (nếu có), được cập nhật thường xuyên;
- Tài liệu thuyết minh tính năng, công dụng của sản phẩm công bố trên bao bì sản phẩm: Báo cáo đầy đủ về Đánh giá tính năng, công dụng của sản phẩm dựa theo thành phần và kết quả thử nghiệm (có tên và chữ ký của đánh giá viên).
TÀI LIỆU HƯỚNG DẪN CỦA ASEAN VỀ KIỂM TRA HẬU MẠI MỸ PHẨM
1. Xây dựng chiến lược kiểm tra hậu mại:
Việc xây dựng chiến lược kiểm tra hậu mại cần căn cứ vào một số yếu tố sau:
a) Dạng sản phẩm: Việc lấy mẫu mỹ phẩm kiểm tra hậu mại cần tập trung vào một số nhóm sản phẩm sau:
- Sản phẩm làm trắng da.
- Phần rôm (bột Talc) hoặc các sản phẩm có chứa khoáng chất.
- Sản phẩm dùng cho mắt, môi.
- Sản phẩm nhuộm tóc, đặc biệt là các sản phẩm xuất xứ từ các nước vẫn cho phép sử dụng một số chất nhuộm nằm trong danh mục các chất cấm sử dụng trong mỹ phảm (Annex II).
- Sản phẩm dành cho trẻ em hoặc phụ nữ có thai.
b) Nguồn gốc xuất xứ của sản phẩm: Cần chú ý các sản phẩm có xuất xứ:
- Từ các nước mà luật khác so với các nước ASEAN.
- Các nước có tiền sử về các sản phẩm không đạt quy định.
c) Công ty, nhãn hàng:
- Dựa vào dữ liệu về tiền sử vi phạm.
- Chú ý các công ty ít tên tuổi, chưa được biết tới.
d) Thành phần:
- Chú ý những nguyên liệu có nguy cơ có thể chứa một số tạp chất gây độc như kim loại nặng, amiăng.
- Một số nguyên liệu có nguy cơ có thể chứa một số tạp chất không được phép ví dụ như TEA độ tinh khiết phải trên 99% (hàm lượng tối đa DEA là 0,5%) hoặc các tạp chất có thể có tương tác với các thành phần khác như tác nhân nitro hoá (các Nitrit trong nước).
2. Khi đánh giá, xem xét mẫu sản phẩm mỹ phẩm, cần chú ý một số chỉ tiêu, thành phần như:
- Sản phẩm làm trắng da: Thủy ngân, hydroquinone, hóc môn (dịch chiết nhau thai).
- Phấn rôm: Kim loại nặng, Asbestos (Amiang), giới hạn vi sinh;
- Sản phẩm trang điểm mắt: Kim loại nặng, giới hạn vi sinh;
- Sản phẩm dùng cho môi: Chất màu cấm sử dụng;
- Sản phẩm nhuộm tóc: Thành phần chất tạo màu cấm sử dụng;
- Các nguyên liệu từ cây cỏ: Dư lượng chất bảo vệ thực vật, vi sinh vật.
3. Kiểm tra Hồ sơ thông tin sản phẩm (PIF):
Khi kiểm tra hồ sơ thông tin sản phẩm cần chú ý những điểm sau:
- Công thức sản phẩm.
- Tiêu chuẩn của nước sử dụng trong sản xuất.
- Sự hiện diện của Benzene trong các Carbomer.
- Hàm lượng Dioxane trong các nguyên liệu ethoxylate hoá, ví dụ như SLES.
- Dầu khoáng/ Vaseline/ Paraffin: phải tuân thủ các yêu cầu trong hướng dẫn của COLIPA về quá trình trưng cất.
- Nguy cơ có nhiễm Nitrosamine (Nitrit trong nước có thể là nguồn của các tác nhân Nitro hoá).
- Đánh giá tính an toàn.
- Những yếu tố liên quan đến chất lượng, ví dụ như quản lý tài liệu, công bố GMP, sự sạch sẽ, vệ sinh trong quá trình sản xuất.
- Các nguyên liệu có nguồn gốc sử dụng công nghệ sinh học (chú ý nguy cơ đột biến gen).
- Dịch chiết thực vật (chú ý dung môi sử dụng, đánh giá tính an toàn, chất bảo vệ thực vật, chất bảo quản).
4. Địa điểm kiểm tra:
Cơ quan quản lý cần lập danh sách các kênh phân phối, đảm bảo không bỏ qua bất kỳ một địa điểm nào. Việc kiểm tra giám sát hậu mại mỹ phẩm cần tập trung nơi đầu nguồn (các đơn vị đầu mối nhập khẩu, phân phối, sản xuất). Ngoài ra, có thể kiểm tra tại các địa điểm:
- Cửa hàng mỹ phẩm
- Cửa hàng ở các trung tâm thương mại
- Nhà thuốc
- Chợ bình dân
- Dịch vụ làm đẹp
- Phòng khám da liễu, ...
- Cơ sở sản xuất không tuân thủ CGMP: căn cứ vào mức độ ảnh hưởng đến chất lượng và tính an toàn của sản phẩm mà có thể yêu cầu doanh nghiệp có biện pháp khắc phục ngay hoặc cần khắc phục trong thời gian ngắn.
Thứ tự ưu tiên trong việc kiểm tra giám sát hậu mại mỹ phẩm dựa vào loại sản phẩm, nguồn gốc xuất xứ, nhãn hàng, thương hiệu công ty, thành phần công thức.
|
TÊN CƠ QUAN LẤY MẪU |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
|
……, ngày … tháng … năm …. |
BIÊN BẢN LẤY MẪU MỸ PHẨM ĐỂ KIỂM TRA CHẤT LƯỢNG
Theo giấy giới thiệu hoặc thẻ thanh tra (ghi rõ số, ngày, tháng, năm và tên cơ quan cấp)
Họ và tên, chức vụ, cơ quan của người tham gia lấy mẫu:
1.................................................................................................................
2.................................................................................................................
3.................................................................................................................
Ngày lấy mẫu:
Tên cơ sở được lấy mẫu: ....................................................................................
Địa chỉ: ............................................................... Điện thoại: ..........................
|
STT |
Tên mỹ phẩm |
Số lô SX, ngày SX, hạn dùng |
Đơn vị đóng gói nhỏ nhất, khối lượng hoặc thể tích |
Số lượng lấy |
Nước sản xuất |
Tên, địa chỉ tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường |
Nhận xét tình trạng lô sản phẩm trước khi lấy mẫu |
|
1 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
… |
|
|
|
|
|
|
|
Điều kiện bảo quản khi lấy mẫu: ...........................................................
Biên bản được làm thành 03 bản: 01 bản lưu tại cơ sở được lấy mẫu, 01 bản lưu tại cơ quan kiểm nghiệm, 01 bản lưu tại cơ quan quản lý kiểm tra chất lượng.
|
Chữ
ký người |
Chữ
ký đại diện cơ sở được |
Chữ
ký người chứng kiến |
CỘNG
HÒA XÃ HỘI CHỦ NGHĨA VIỆT NAM
Độc lập - Tự do - Hạnh phúc
-------------
PHIẾU ĐĂNG KÝ QUẢNG CÁO MỸ PHẨM, TỔ CHỨC HỘI THẢO, SỰ KIỆN GIỚI THIỆU MỸ PHẨM
Số: ....
Kính gửi: Sở Y tế tỉnh/ thành phố ....
1. Tên đơn vị đăng ký hồ sơ:
2. Địa chỉ:
3. Số điện thoại, Fax, E-mail:
4. Số giấy phép hoạt động (giấy chứng nhận đăng ký kinh doanh):
5. Tên, số điện thoại của người hoặc bộ phận chịu trách nhiệm đăng ký hồ sơ:
6. Danh mục mỹ phẩm đăng ký quảng cáo, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm:
|
STT |
Tên mỹ phẩm |
Số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm |
Hình thức quảng cáo (đối với hồ sơ đăng ký quảng cáo mỹ phẩm) |
Thời gian, địa điểm dự kiến tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm (đối với hồ sơ đăng ký tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm) |
Lần thứ |
|
1 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
… |
|
|
|
|
|
7. Tài liệu gửi kèm:
- Nội dung (dự kiến) quảng cáo hoặc tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm của từng sản phẩm.
- Bản sao Phiếu công bố sản phẩm mỹ phẩm đã được cấp số tiếp nhận.
8. Cam kết của đơn vị đăng ký quảng cáo mỹ phẩm:
Chúng tôi đã nghiên cứu kỹ Thông tư Quy định về quản lý mỹ phẩm số ... ngày ... tháng ... năm … của Bộ Y tế và cam kết sẽ tuân thủ các quy định của Thông tư này vì sức khoẻ và lợi ích của người sử dụng mỹ phẩm.
|
|
... , ngày ...
tháng ... năm ... |
|
UBND TỈNH/ TP |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: ………… |
|
PHIẾU TIẾP NHẬN HỒ SƠ ĐĂNG KÝ QUẢNG CÁO MỸ PHẨM, TỔ CHỨC HỘI THẢO, SỰ KIỆN GIỚI THIỆU MỸ PHẨM
Sở Y tế tỉnh/ thành phố ... đã tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm số: (ghi số phiếu đăng ký hồ sơ quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm của đơn vị)
Của đơn vị: (ghi tên đơn vị nộp hồ sơ)
Địa chỉ: (ghi địa chỉ của đơn vị nộp hồ sơ)
Điện thoại: (ghi số điện thoại của đơn vị nộp hồ sơ)
Tên sản phẩm mỹ phẩm đăng ký quảng cáo, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm:
Hình thức quảng cáo: (đối với hồ sơ đăng ký quảng cáo)
Ngày nhận đủ hồ sơ hợp lệ: (Ngày/ tháng/ năm)
Số Phiếu tiếp nhận (*):
|
|
... , ngày ...
tháng ... năm ... |
(*) Ghi chú: Cách ghi số Phiếu tiếp nhận là a/XX/QCMP-A, trong đó:
- a là Số Phiếu tiếp nhận;
- XX là hai chữ số cuối của năm cấp;
- QCMP là các ký tự viết tắt của cụm từ "quảng cáo mỹ phẩm";
- A là ký hiệu viết tắt tên tỉnh, thành phố được quy định tại Phụ lục số 04-MP.
Ví dụ: 268/11/QCMP-HN có nghĩa là số Phiếu tiếp nhận hồ sơ quảng cáo mỹ phẩm là 268 do Sở Y tế Hà Nội cấp năm 2011.
SOCIALIST
REPUBLIC OF VIETNAM
Independence - Freedom - Happiness
---------------
(PROVINCIAL/MUNICIPAL) PEOPLE’S COMMITTEE
(PROVINCIAL/MUNICIPAL) HEALTH SERVICE
Address:
Tel: Fax:
No.: ... /CFS
Date ...
TO WHOM IT MAY CONCERN
We, (PROVINCIAL/MUNICIPAL) HEALTH SERVICE, hereby certify that the following product manufactured by (Manufacturer’s name) is allowed to be sold freely in Viet Nam.
- Manufacturer:
- Address:
- Kind of product: Cosmetics
- Name of product:
|
|
AUTHORISED
SIGNATURE Director |
|
TÊN ĐƠN VỊ |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: |
…, ngày … tháng … năm …. |
PHIẾU ĐĂNG KÝ KIỂM TRA THỰC HÀNH TỐT SẢN XUẤT MỸ PHẨM
Kính gửi: Cục Quản lý dược - Bộ Y tế
138A Giảng Võ, Ba Đình, Hà Nội
1- Tên cơ sở:
2- Địa chỉ:
3- Điện thoại: Fax: E-Mail:
Thực hiện Thông tư Quy định về quản lý mỹ phẩm số ... ngày .... tháng.... năm... của Bộ Y tế, sau khi tiến hành tự thanh tra và đánh giá đạt tiêu chuẩn “Thực hành tốt sản xuất mỹ phẩm”, Cơ sở chúng tôi xin đăng ký với Cục Quản lý dược được kiểm tra CGMP-ASEAN.
Xin gửi kèm bản đăng ký này các tài liệu liên quan sau đây:
1. Giấy Chứng nhận đăng ký kinh doanh hoặc giấy phép đầu tư.
2. Sơ đồ tổ chức, nhân sự của cơ sở.
3. Tài liệu đào tạo về “Thực hành tốt sản xuất mỹ phẩm”.
4. Sơ đồ vị trí và thiết kế của nhà máy, bao gồm sơ đồ mặt bằng tổng thể; sơ đồ đường đi của công nhân; sơ đồ đường đi của nguyên liệu, bao bì, bán thành phẩm, thành phẩm; sơ đồ hệ thống cung cấp nước phục vụ sản xuất; sơ đồ xử lý chất thải.
5. Danh mục thiết bị hiện có của cơ sở.
6. Danh mục các mặt hàng đang sản xuất hoặc dự kiến sản xuất.
7. Biên bản tự thanh tra “Thực hành tốt sản xuất mỹ phẩm”.
|
|
GIÁM ĐỐC ĐƠN VỊ |
|
TÊN ĐƠN VỊ |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: |
…, ngày … tháng … năm …. |
ĐƠN HÀNG NHẬP KHẨU MỸ PHẨM DÙNG CHO NGHIÊN CỨU, KIỂM NGHIỆM
Kính gửi: Cục Quản lý dược - Bộ Y tế
138A Giảng Võ, Ba Đình, Hà Nội
(Đơn vị) kính đề nghị Cục Quản lý dược xét duyệt để đơn vị được nhận các mỹ phẩm dùng cho kiểm nghiệm chất lượng sau:
|
STT |
Tên mỹ phẩm, dạng bào chế, quy cách đóng gói |
Dạng sản phẩm |
Thành phần |
Đơn vị tính |
Số lượng |
Tên công ty sản xuất, tên nước |
Ghi chú |
|
1 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cục Quản lý dược Chấp thuận đơn hàng nhập khẩu gồm … trang … khoản kèm theocông văn số … /QLD-CL … ngày … tháng … năm … của Cục Quản lý dược. Hà Nội, ngày …
tháng … năm … |
...
, ngày ... tháng ... năm ...
|
|
UBND TỈNH/ TP |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: ………. |
... , ngày ... tháng ... năm ... |
DANH SÁCH CÁC SẢN PHẨM ĐÃ CẤP SỐ TIẾP NHẬN PHIẾU CÔNG BỐ SẢN PHẨM MỸ PHẨM
Từ tháng ... đến tháng ... năm ...
Kính gửi: Cục Quản lý dược - Bộ Y tế
138 A Giảng Võ, Ba Đình, Hà Nội
Sở Y tế tỉnh/ thành phố ... (hoặc Ban Quản lý...) báo cáo danh sách các mỹ phẩm đã được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm từ tháng ... đến tháng ... năm ... như sau:
|
STT |
Tên sản phẩm |
Dạng sản phẩm |
Đơn
vị công bố |
Số
tiếp nhận |
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
|
|
... |
|
|
|
|
|
Tổng số |
|
|
|
|
|
|
THỦ TRƯỞNG CƠ QUAN |
|
UBND TỈNH/ TP |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: ………. |
... , ngày ... tháng ... năm ... |
Từ tháng ... đến tháng ... năm ...
Kính
gửi: Cục Quản lý dược - Bộ Y tế
138A Giảng Võ, Ba Đình, Hà Nội
Sở Y tế tỉnh/ thành phố ... (hoặc Ban Quản lý...) báo cáo danh sách mỹ phẩm đã cấp Phiếu tiếp nhận hồ sơ đăng ký quảng cáo mỹ phẩm, tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm từ tháng ... đến tháng ... năm ... như sau:
1. Hồ sơ đăng ký quảng cáo mỹ phẩm:
|
STT |
Tên sản phẩm |
Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường |
Đơn vị đăng ký quảng cáo |
Hình thức quảng cáo |
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
... |
|
|
|
|
|
Tổng số |
|
|
|
|
2. Hồ sơ đăng ký tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm:
|
STT |
Tên sản phẩm |
Tổ chức, cá nhân chịu trách nhiệm đưa sản phẩm ra thị trường |
Đơn vị đăng ký tổ chức hội thảo, sự kiện giới thiệu mỹ phẩm |
|
1 |
|
|
|
|
2 |
|
|
|
|
... |
|
|
|
|
Tổng số |
|
|
|
|
|
THỦ TRƯỞNG CƠ QUAN |
|
TÊN ĐƠN VỊ |
CỘNG HÒA XÃ HỘI CHỦ
NGHĨA VIỆT NAM |
|
Số: ... |
... , ngày …. tháng ... năm ... |
BÁO CÁO KẾT QUẢ HOẠT ĐỘNG SẢN XUẤT, KINH DOANH MỸ PHẨM
Năm ...
|
Kính gửi: |
- Cục Quản lý dược - Bộ Y tế |
(Đơn vị) ... báo cáo hoạt động sản xuất, kinh doanh năm ... của đơn vị như sau:
1. Tổng số sản phẩm đã công bố:
2. Số mặt hàng sản xuất/ nhập khẩu kinh doanh năm ...:
3. Sản lượng hàng hóa sản xuất/ nhập khẩu kinh doanh năm ...: (phân theo nhóm sản phẩm)
4. Khó khăn vướng mắc của đơn vị:
5. Đề xuất, kiến nghị (nếu có).
|
|
GIÁM ĐỐC ĐƠN VỊ |
Kính
gửi: Cục Quản lý dược - Bộ Y tế
138A Giảng Võ, Ba Đình, Hà Nội
THÔNG BÁO TÁC DỤNG BẤT LỢI
I. Thông tin về công ty
|
Tên và địa chỉ của công ty |
|
|
|
Tên và chức danh người thông báo |
|
|
|
Số điện thoại: |
Fax: |
Email: |
II. Thông tin sản phẩm
|
Tên sản phẩm (giống như tên trên đơn công bố) |
|
|
Danh sách thành phần, dạng đóng gói |
(Đính kèm theo danh sách thành phần riêng biệt) |
|
Dạng sản phẩm/ mục đích sử dụng |
|
|
Tên công ty sản xuất/ xuất xứ |
|
|
Ngày sản xuất hoặc hạn dùng |
|
|
Số lô |
|
III. Báo cáo tác dụng bất lợi chi tiết
|
Tên người sử dụng |
|
||
|
Số chứng minh nhân dân hoặc hộ chiếu |
|
||
|
Tuổi |
|
Giới tính |
|
|
Tôn giáo/Quốc tịch |
|
||
|
Thời gian xuất hiện tác dụng bất lợi |
|
||
|
Mô tả tác dụng bất lợi (đính kèm bản mô tả tác dụng bất lợi nếu cần thiết) Thời gian giữa lần dùng sản phẩm cuối cùng và thời điểm xuất hiện tác dụng bất lợi: ___phút ___giờ __ ngày Sản phẩm đó được sử dụng như thế nào: |
|||
|
Người sử dụng có phải nhập viện vì tác dụng bất lợi không?
|
# Có # Không
|
||
|
Người sử dụng cú phải điều trị y tế không? |
# Có # Không
|
||
|
Kết quả # Đã hồi phục (Ngày: _____) # Tử vong (Ngày: _______) # Vẫn chưa hồi phục # Không biết |
|||
|
Nguồn cung cấp báo cáo |
# Chuyên gia y tế (đề nghị ghi rõ) # Khách hàng # Nguồn khác (đề nghị ghi rõ) |
||
[Chữ ký của người báo cáo tác dụng bất lợi/ ngày tháng năm ]
1 Thông tư số 29/2020/TT-BYT ngày 31 tháng 12 năm 2020 của Bộ trưởng Bộ Y tế sửa đổi, bổ sung và bãi bỏ một số văn bản quy phạm pháp luật do Bộ trưởng Bộ Y tế ban hành, liên tịch ban hành có căn cứ ban hành như sau:
"Căn cứ Luật ban hành văn bản quy phạm pháp luật ngày 22 tháng 6 năm 2015 và Luật sửa đổi, bổ sung một số điều của Luật ban hành văn bản quy phạm pháp luật ngày 18 tháng 6 năm 2020;
Căn cứ Luật dược ngày 06 tháng 4 năm 2016;
Căn cứ Nghị định số 54/2017/NĐ-CP ngày 08 tháng 5 năm 2017 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược;
Căn cứ Nghị định số 69/2018/NĐ-CP ngày 15 tháng 5 năm 2018 của Chính phủ quy định chi tiết một số điều của Luật Quản lý ngoại thương;
Căn cứ Nghị định số 96/2012/NĐ-CP ngày 15 tháng 11 năm 2012 của Chính phủ quy định về điều trị nghiện các chất dạng thuốc phiện bằng thuốc thay thế;
Căn cứ Nghị định số 15/2018/NĐ-CP ngày 02 tháng 02 năm 2018 của Chính phủ quy định chi tiết thi hành một số điều của Luật an toàn thực phẩm;
Căn cứ Nghị định số 34/2016/NĐ-CP ngày 14 tháng 5 năm 2016 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật Ban hành văn bản quy phạm pháp luật;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Theo đề nghị của Vụ trưởng Vụ Pháp chế,
Bộ trưởng Bộ Y tế ban hành Thông tư sửa đổi, bổ sung và bãi bỏ một số văn bản quy phạm pháp luật do Bộ trưởng Bộ Y tế ban hành, liên tịch ban hành."
2 Khoản này được bãi bỏ theo quy định tại Khoản 2 Điều 12 Nghị định số 155/2018/NĐ-CP ngày 12/11/2018 của Chính phủ sửa đổi, bổ sung một số quy định liên quan đến điều kiện đầu tư kinh doanh thuộc phạm vi quản lý nhà nước của Bộ Y tế, có hiệu lực kể từ ngày 12 tháng 11 năm 2018.
3 Khoản này được sửa đổi, bổ sung theo quy định tại điểm a Khoản 1 Điều 1 Thông tư số 29/2020/TT-BYT, có hiệu lực thi hành kể từ ngày 15 tháng 02 năm 2021.
4 Chương này được bãi bỏ theo quy định tại Khoản 2 Điều 24 Thông tư số 09/2015/TT-BYT ngày 25/5/2015 của Bộ trưởng Bộ Y tế quy định về xác nhận nội dung quảng cáo đối với sản phẩm, hàng hóa, dịch vụ đặc biệt thuộc lĩnh vực quản lý của Bộ Y tế, có hiệu lực thi hành kể từ ngày 16 tháng 7 năm 2015.
5 Điều này được sửa đổi, bổ sung theo quy định tại điểm c Khoản 1 Điều 1 Thông tư số 29/2020/TT-BYT, có hiệu lực thi hành kể từ ngày 15 tháng 02 năm 2021.
6 Điểm này được bãi bỏ theo quy định tại Khoản 2 Điều 12 Nghị định số 155/2018/NĐ-CP, có hiệu lực thi hành kể từ ngày 12 tháng 11 năm 2018.
7 Điểm này được bãi bỏ theo quy định tại Khoản 2 Điều 12 Nghị định số 155/2018/NĐ-CP, có hiệu lực thi hành kể từ ngày 12 tháng 11 năm 2018.
8 Điểm này được bãi bỏ theo quy định tại Khoản 2 Điều 12 Nghị định số 155/2018/NĐ-CP, có hiệu lực thi hành kể từ ngày 12 tháng 11 năm 2018.
9 Khoản này được bãi bỏ theo quy định tại Khoản 2 Điều 12 Nghị định số 155/2018/NĐ-CP, có hiệu lực thi hành kể từ ngày 12 tháng 11 năm 2018.
10 Điều 3, Điều 4, Điều 5 của Thông tư số 29/2020/TT-BYT, có hiệu lực thi hành kể từ ngày 15 tháng 02 năm 2021 quy định như sau:
"Điều 3. Hiệu lực thi hành
1. Thông tư này có hiệu lực thi hành từ ngày 15 tháng 02 năm 2021.
2. Riêng các quy định tại các khoản 5, 6, 7, 8 và 11 Điều 1 Thông tư này có hiệu lực từ ngày 01 tháng 01 năm 2021.
3. Các quy định liên quan đến nộp hồ sơ, tài liệu và tra cứu trực tuyến được áp dụng trong giai đoạn dịch Covid - 19 cho đến thời điểm Bộ Y tế xem xét, điều chỉnh phù hợp với yêu cầu thực tiễn.
Điều 4. Quy định chuyển tiếp
1. Các hồ sơ đã nộp cho cơ quan tiếp nhận hồ sơ trước ngày Thông tư này có hiệu lực nhưng đang trong quá trình giải quyết được áp dụng theo quy định có liên quan tại Thông tư này hoặc các quy định trước ngày Thông tư này có hiệu lực theo hướng thuận tiện cho doanh nghiệp, tổ chức, cá nhân.
2. Các quy định về công bố thông tin, cập nhật, khai báo và báo cáo theo hình thức trực tuyến tại Thông tư này được áp dụng theo triển khai của cơ quan nhà nước có thẩm quyền.
Điều 5. Trách nhiệm thi hành
Vụ trưởng Vụ Pháp chế, Chánh Văn phòng Bộ, Chánh Thanh tra Bộ, Vụ trưởng, Cục trưởng, Tổng Cục trưởng các Vụ, Cục, Tổng cục thuộc Bộ Y tế và các cơ quan, tổ chức, cá nhân có liên quan chịu trách nhiệm thi hành Thông tư này./."
11 Phụ lục này được sửa đổi, bổ sung theo quy định tại điểm b Khoản 1 Điều 1 Thông tư số 29/2020/TT-BYT, có hiệu lực thi hành kể từ ngày 15 tháng 02 năm 2021.
1 Như đã được định nghĩa rõ ràng trong tài liệu hướng dẫn cho các công ty về báo cáo tác dụng phụ của sản phẩm mỹ phẩm.
As defined in the Guide Manual for the Industry on Adverse Event Reporting of Cosmetics Products.
2 Trình bày trong phụ lục I trong tài liệu hướng dẫn cho các công ty về báo cáo tác dụng phụ của sản phẩm mỹ phẩm.
Set out in Appendix I to the Guide Manual for the Industry on Adverse Event Reporting of Cosmetics Products.
(Không có nội dung)
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
(Không có nội dung)
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
-
Ban hành: {{m.News_Dates_Date}} Hiệu lực: {{m.News_EffectDate_Date}} Tình trạng: {{m.TinhTrang}} Cập nhật: {{m.Email_SendDate_Date}} Ban hành: {{m.News_Dates_Date}}Hiệu lực: {{m.News_EffectDate_Date}}Tình trạng: {{m.TinhTrang}}Cập nhật: {{m.Email_SendDate_Date}}
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
-
Ban hành: {{m.News_Dates_Date}} Hiệu lực: {{m.News_EffectDate_Date}} Tình trạng: {{m.TinhTrang}} Cập nhật: {{m.Email_SendDate_Date}} Ban hành: {{m.News_Dates_Date}}Hiệu lực: {{m.News_EffectDate_Date}}Tình trạng: {{m.TinhTrang}}Cập nhật: {{m.Email_SendDate_Date}}
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây