Quyết định 127/QĐ-BYT năm 2019 về \"hướng dẫn thực hiện giám sát quốc gia về kháng kháng sinh\" do Bộ trưởng Bộ Y tế ban hành
Quyết định 127/QĐ-BYT năm 2019 về \"hướng dẫn thực hiện giám sát quốc gia về kháng kháng sinh\" do Bộ trưởng Bộ Y tế ban hành
| Số hiệu: | 127/QĐ-BYT | Loại văn bản: | Quyết định |
| Nơi ban hành: | Bộ Y tế | Người ký: | Nguyễn Viết Tiến |
| Ngày ban hành: | 15/01/2019 | Ngày hiệu lực: | Đã biết |
| Ngày công báo: | Đang cập nhật | Số công báo: | Đang cập nhật |
| Tình trạng: | Đã biết |
| Số hiệu: | 127/QĐ-BYT |
| Loại văn bản: | Quyết định |
| Nơi ban hành: | Bộ Y tế |
| Người ký: | Nguyễn Viết Tiến |
| Ngày ban hành: | 15/01/2019 |
| Ngày hiệu lực: | Đã biết |
| Ngày công báo: | Đang cập nhật |
| Số công báo: | Đang cập nhật |
| Tình trạng: | Đã biết |
|
BỘ Y TẾ |
CỘNG HÒA XÃ
HỘI CHỦ NGHĨA VIỆT NAM |
|
Số: 127/QĐ-BYT |
Hà Nội, ngày 15 tháng 01 năm 2019 |
VỀ VIỆC BAN HÀNH “HƯỚNG DẪN THỰC HIỆN GIÁM SÁT QUỐC GIA VỀ KHÁNG KHÁNG SINH”
BỘ TRƯỞNG BỘ Y TẾ
Căn cứ Luật Khám bệnh, chữa bệnh năm 2009;
Căn cứ Nghị định số 75/2017/NĐ-CP ngày 20 tháng 6 năm 2017 của Chính phủ quy định chức năng, nhiệm vụ, quyền hạn và cơ cấu tổ chức của Bộ Y tế;
Theo đề nghị của Cục trưởng Cục Quản lý khám, chữa bệnh,
QUYẾT ĐỊNH:
Điều 1. Ban hành kèm theo Quyết định này “Hướng dẫn thực hiện giám sát quốc gia về kháng kháng sinh”.
Điều 2. “Hướng dẫn thực hiện giám sát quốc gia về kháng kháng sinh” được áp dụng tại các cơ sở khám bệnh, chữa bệnh trong Mạng lưới giám sát kháng thuốc và khuyến khích áp dụng tại các cơ sở khám bệnh, chữa bệnh khác.
Điều 3. Quyết định này có hiệu lực kể từ ngày ký, ban hành.
Điều 4. Các ông, bà: Chánh Văn phòng Bộ, Chánh thanh tra Bộ, Tổng Cục trưởng, Cục trưởng và Vụ trưởng các Tổng cục, Cục, Vụ thuộc Bộ Y tế, Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc trung ương, Giám đốc các Bệnh viện, Viện trực thuộc Bộ Y tế, Thủ trưởng Y tế các ngành chịu trách nhiệm thi hành Quyết định này./.
|
|
KT. BỘ
TRƯỞNG |
THỰC
HIỆN GIÁM SÁT QUỐC GIA VỀ KHÁNG KHÁNG SINH
(Ban hành kèm theo Quyết định số 127/QĐ-BYT ngày 15 tháng 01 năm 2019 của Bộ
trưởng Bộ Y tế)
MỤC LỤC
GIỚI THIỆU
Tổng quan
Khung chính sách
Mục tiêu giám sát
Lộ trình
Đơn vị giám sát kháng thuốc
CHƯƠNG 1. PHƯƠNG PHÁP GIÁM SÁT
1. Quần thể
2. Phương pháp vi khuẩn học và kháng sinh đồ (AST)
3. Nhập dữ liệu vào WHONET
4. Dữ liệu phải báo cáo cho VNASS
5. Loại bỏ các dữ liệu trùng lặp
6. Gửi dữ liệu đến Đơn vị AMR
CHƯƠNG 2: CÁC TÁC NHÂN ƯU TIÊN, BỆNH PHẨM VÀ AST ĐỂ PHÂN TÍCH DỮ LIỆU
Tác nhân gây bệnh và bệnh phẩm lâm sàng
CHƯƠNG 3: CÁC TIÊU CHUẨN TRONG GIÁM SÁT VÀ BÁO CÁO
1. Các phòng xét nghiệm Vi sinh
2. Đơn vị AMR
1. Chất lượng và tính đầy đủ của dữ liệu:
2. Chỉ số chất lượng phòng xét nghiệm:
PHỤ LỤC A1
DANH MỤC KHÁNG SINH THỬ NGHIỆM TỐI THIỂU
CHO CÁC TÁC NHÂN GÂY BỆNH ƯU TIÊN
PHỤ LỤC B:
BÁO CÁO VỀ QUẦN THỂ VÀ THU THẬP DỮ LIỆU NUÔI CẤY HÀNG THÁNG
PHỤ LỤC C:
HƯỚNG DẪN CÁCH TẢI MỘT TỆP TIN WHONET
LÊN CỔNG THÔNG TIN ĐIỆN TỬ AMR: kks.kcb.vn
1. Giới thiệu
2. Đăng nhập
3. Bảng hiển thị
4. Nhập và gửi báo cáo
CÁC CHỮ VIẾT TẮT
|
AMR |
Antimicrobial resistance Kháng kháng kháng sinh |
|
AST |
Antimicrobial susceptibility testing Kháng sinh đồ |
|
ATCC |
American Type Culture Collection Các chủng chuẩn |
|
CLSI |
Clinical & Laboratory Standards Institute Viện Tiêu chuẩn Lâm sàng và Xét nghiệm |
|
EQA |
External quality assurance Ngoại kiểm |
|
GLASS |
Global Antimicrobial Resistance Surveillance System Hệ thống giám sát kháng thuốc toàn cầu |
|
IPC |
Infection Prevention and Control Kiểm soát nhiễm khuẩn |
|
MOH |
Ministry of Health Bộ Y tế |
|
NCC |
National coordinating center Trung tâm Điều phối quốc gia |
|
QC |
Quality control Kiểm soát chất lượng |
|
VAMS |
Viet Nam Administration for Medical Services Cục Quản lý Khám, chữa bệnh |
|
VNASS |
Viet Nam Antimicrobial Resistance Surveillance System Hệ thống giám sát kháng kháng sinh Việt Nam |
|
WHO |
World Health Organization Tổ chức Y tế Thế giới |
Tổng quan
Kháng kháng sinh đang là mối đe dọa sức khỏe toàn cầu. Kháng sinh là một trong những phương pháp điều trị bệnh quan trọng trong nền y học hiện đại, giúp điều trị hiệu quả các nhiễm trùng đe dọa tính mạng con người và giúp phòng ngừa các biến chứng nhiễm trùng từ các can thiệp y tế và phẫu thuật thông thường. Tuy nhiên, sự xuất hiện của các vi khuẩn kháng kháng sinh đã gây nên mối đe dọa tính mạng người bệnh do các vi khuẩn gia tăng đề kháng đối với nhiều loại kháng sinh và trong một số trường hợp kháng với tất cả các kháng sinh hiện có.
Trong thời đại đi lại toàn cầu, nhiều dạng đề kháng có thể lây lan dễ dàng từ khu vực này sang khu vực khác, và khi xuất hiện đề kháng ở bất cứ một nơi nào cũng là mối đe dọa đề kháng trên toàn cầu. Cộng đồng y tế toàn cầu đã thừa nhận tính cấp bách của cuộc khủng hoảng về kháng kháng sinh, và năm 2015, Hội đồng Y tế Thế giới đã thông qua Kế hoạch hành động toàn cầu về phòng chống kháng kháng sinh.
Việt Nam tham gia vào mạng lưới phòng chống kháng kháng sinh trên toàn cầu nhằm hiểu rõ và hạn chế mối đe dọa của kháng kháng sinh. Ở Việt Nam, mỗi năm số trường hợp nhiễm vi khuẩn kháng kháng sinh là khá lớn (tuy chưa có con số thống kê cụ thể), trong số đó có nhiều trường hợp do nhiễm tại các cơ sở y tế. Điều này dẫn tới các nguy cơ không thể chấp nhận về an toàn người bệnh cũng như đã tạo ra gánh nặng đáng kể cho hệ thống y tế của Việt Nam.
Tuy nhiên, mức độ kháng kháng sinh thâm nhập và lây lan ở Việt Nam vẫn chưa được hiểu đầy đủ. Việt Nam đã cam kết triển khai thực hiện một Hệ thống giám sát kháng kháng sinh chuẩn hóa để hiểu rõ hơn về mối đe dọa kháng kháng sinh và tăng cường các nỗ lực để giảm thiểu mối đe dọa này.
Khung chính sách
Kế hoạch hành động quốc gia năm 2013 về Phòng, chống kháng thuốc giai đoạn 2013 - 2020 đã nêu ra cam kết của Chính phủ Việt Nam trong việc tăng cường giám sát quốc gia đối với các vi sinh vật kháng thuốc, trong đó có cam kết Kế nâng cao nhận thức trong cộng đồng và ngành y tế về nguy cơ kháng kháng sinh không được kiểm soát ở Việt Nam. Kế hoạch hành động đã nêu ra giải pháp đa phương thức bao gồm đảm bảo cung cấp đủ thuốc có chất lượng, đẩy mạnh sử dụng kháng sinh an toàn, hợp lý trong y học, tăng cường các biện pháp phòng ngừa và kiểm soát nhiễm khuẩn cũng như sử dụng kháng sinh an toàn hợp lý cho gia súc, gia cầm và trong nuôi trồng thủy sản. Năm 2013, Dự án kháng thuốc VINARES hợp tác giữa Đơn vị nghiên cứu lâm sàng của Đại học Oxford (Oxford University Clinical Research Unit - OUCRU) và 16 phòng xét nghiệm trên cả nước đã triển khai nhằm giải quyết các vấn đề về kháng kháng sinh trong lĩnh vực y tế và bước đầu thiết lập mạng lưới giám sát kháng kháng sinh.
Ngày 17 tháng 10 năm 2016, Bộ Y tế đã ban hành Quyết định 6211/QĐ-BYT về việc thiết lập và quy định chức năng, nhiệm vụ của mạng lưới giám sát vi khuẩn kháng thuốc tại các cơ sở khám, chữa bệnh. Quyết định này là nền tảng trong thiết lập hệ thống giám sát vi khuẩn kháng thuốc trong các cơ sở y tế, bao gồm 16 phòng xét nghiệm trọng điểm trong mạng lưới giám sát kháng kháng sinh trong giai đoạn triển khai ban đầu (Bảng 1). Quyết định 6211/QĐ-BYT nêu lên vai trò, trách nhiệm của hệ thống giám sát.
Bảng 1. Các cơ sở giám sát trọng điểm trong giai đoạn triển khai ban đầu
|
Tên bệnh viện |
Tỉnh/Thành phố |
Khu vực |
|
1. Bệnh viện Bạch Mai |
Hà Nội |
Miền Bắc |
|
2. Bệnh viện Bệnh nhiệt đới trung ương |
Hà Nội |
Miền Bắc |
|
3. Bệnh viện Nhi Trung ương |
Hà Nội |
Miền Bắc |
|
4. Bệnh viện Hữu nghị Việt Đức |
Hà Nội |
Miền Bắc |
|
5. Bệnh viện đa khoa Xanh Pôn |
Hà Nội |
Miền Bắc |
|
6. Bệnh viện Hữu nghị Việt Tiệp |
Hải Phòng |
Miền Bắc |
|
7. Bệnh viện Việt Nam - Thụy Điển, Uông Bí |
Quảng Ninh |
Miền Bắc |
|
8. Bệnh viện Trung ương Huế |
Huế |
Miền Trung |
|
9. Bệnh viện đa khoa Đà Nẵng |
Đà Nẵng |
Miền Trung |
|
10. Bệnh viện đa khoa tỉnh Bình Định |
Bình Định |
Miền Trung |
|
11. Bệnh viện đa khoa tỉnh ĐakLak |
Đắk Lắk |
Miền Trung |
|
12. Bệnh viện đa khoa tỉnh Khánh Hòa |
Khánh Hòa |
Miền Trung |
|
13. Bệnh viện Chợ Rẫy |
Hồ Chí Minh |
Miền Nam |
|
14. Bệnh viện Bệnh Nhiệt đới TP Hồ Chí Minh |
Hồ Chí Minh |
Miền Nam |
|
15. Bệnh viện Nhi Đồng 1 |
Hồ Chí Minh |
Miền Nam |
|
16. Bệnh viện đa khoa Trung ương Cần Thơ |
Cần Thơ |
Miền Nam |
Mục tiêu giám sát
Mục tiêu thiết lập Hệ thống giám sát quốc gia về kháng kháng sinh (Viet Nam Antimicrobial Resistance Surveillance System - viết tắt là VNASS) là thực hiện việc thu thập, phân tích và chia sẻ dữ liệu đã được chuẩn hóa nhằm đưa ra các khuyến cáo hành động ở cấp địa phương, quốc gia, và toàn cầu để giảm thiểu tình trạng kháng kháng sinh. Mục tiêu cụ thể của Hệ thống giám sát bao gồm:
• Xác định đặc điểm tác nhân gây bệnh tại các bệnh viện.
• Theo dõi thay đổi về mô hình đề kháng theo thời gian và phát hiện các tác nhân gây bệnh kháng kháng sinh mới nổi.
• Nâng cao năng lực của các phòng xét nghiệm vi sinh về thực hiện xét nghiệm định danh và kháng sinh đồ chuẩn thức để phát hiện các tác nhân gây bệnh.
• Cung cấp thông tin về chính sách kiểm soát nhiễm khuẩn quốc gia.
• Thực hiện các hoạt động kiểm soát nhiễm khuẩn theo mục tiêu tại các bệnh viện dựa trên dữ liệu kháng kháng sinh của địa phương.
• Phân tích và chia sẻ dữ liệu kháng kháng sinh ở cấp độ quốc gia và toàn cầu bằng báo cáo cho GLASS - Mạng lưới báo cáo kháng kháng sinh toàn cầu của Tổ chức Y tế thế giới (WHO).
Để triển khai hệ thống giám sát quốc gia về kháng kháng sinh đạt các mục tiêu đề ra, Bộ Y tế xây dựng tài liệu Hướng dẫn thực hiện giám sát kháng kháng sinh. Tài liệu này nêu ra giải pháp về thực hiện sớm giám sát kháng kháng sinh chuẩn hóa ở Việt Nam, bao gồm phương pháp giám sát; vai trò và trách nhiệm tại cấp cơ sở, khu vực và quốc gia; và các yêu cầu về thu thập, quản lý và báo cáo dữ liệu. Đối tượng sử dụng tài liệu này là 16 phòng xét nghiệm trọng điểm, là những đơn vị của Hệ thống giám sát kháng kháng sinh trong giai đoạn triển khai ban đầu.
Lộ trình
Hệ thống giám sát kháng kháng sinh được thành lập với sự tham gia của 16 phòng xét nghiệm từ Dự án VINARES. Mỗi phòng xét nghiệm đã được đánh giá sơ bộ về năng lực xét nghiệm vi sinh, bao gồm các quy trình vi sinh, nguồn nhân lực, cơ sở hạ tầng, trang thiết bị và hệ thống thông tin. Một số khóa tập huấn và đào tạo tại cơ sở và khu vực đã được triển khai và sẽ tiếp tục được tổ chức để khắc phục các tồn tại đã được xác định trong đánh giá này, với ưu tiên trọng điểm là nâng cao năng lực xét nghiệm về định danh vi khuẩn, kháng sinh đồ và thực hiện nội kiểm cho các phòng xét nghiệm vi sinh.
16 Cơ sở trọng điểm đã ứng dụng phần mềm quản lý dữ liệu vi sinh- WHONET thông qua Dự án VINARES. Đây là một phần mềm đa ngôn ngữ miễn phí được xây dựng bởi Trung tâm Hợp tác về giám sát kháng kháng sinh của Tổ chức Y tế thế giới và được sử dụng làm nền tảng giám sát cho VNASS. Các phòng xét nghiệm sẽ nhận được các phản hồi, phân tích sơ bộ dữ liệu giám sát, hỗ trợ kỹ thuật để kết nối WHONET vào luồng dữ liệu thường quy của phòng xét nghiệm, chuẩn hóa báo cáo và cải thiện chất lượng dữ liệu trong các năm đầu thực hiện. Khi dữ liệu chuẩn hóa được báo cáo cho VNASS một cách nhất quán, các kết quả giám sát sẽ được chia sẻ đến cấp độ quốc gia và tới GLASS hàng năm. Các bên liên quan cũng sẽ họp định kỳ để đánh giá quá trình và trao đổi ý tưởng về các định hướng tương lai cho Hệ thống giám sát.
Đơn vị giám sát kháng thuốc
Đơn vị giám sát kháng thuốc (viết tắt là Đơn vị AMR) tại Cục Quản lý Khám, chữa bệnh sẽ là trung tâm điều phối quốc gia của VNASS. Đơn vị AMR gồm các chuyên viên về bệnh truyền nhiễm, dịch tễ học, vi sinh và công nghệ thông tin, chịu trách nhiệm:
- Xây dựng các phương pháp giám sát và các yêu cầu báo cáo giám sát kháng kháng sinh.
- Xác nhận việc tuân thủ các chương trình nội kiểm và ngoại kiểm xem xét kết quả ngoại kiểm của các phòng xét nghiệm trong hệ thống giám sát.
- Tiếp nhận và quản lý dữ liệu giám sát từ tất cả các phòng xét nghiệm của mạng lưới
- Phản hồi các yêu cầu của phòng xét nghiệm.
- Đơn vị AMR sẽ đáp ứng các nhu cầu đào tạo và hỗ trợ kỹ thuật cho các phòng xét nghiệm trong Hệ thống. Đơn vị AMR sẽ phối hợp với các chuyên gia vi sinh trong nước, quốc tế, hoặc nhóm kỹ thuật về AMR quốc gia để xây dựng các chính sách, quyết định, hướng dẫn về giám sát kháng kháng sinh.
CHƯƠNG 1. PHƯƠNG PHÁP GIÁM SÁT
1. Quần thể
Quần thể bệnh nhân của 16 điểm giám sát trọng điểm bao gồm tất cả các bệnh nhân các nhóm tuổi trên khắp các khu vực Bắc, Trung, Nam trong cả nước. Các phòng xét nghiệm trong Hệ thống giám sát sẽ được yêu cầu cung cấp toàn bộ dữ liệu bệnh nhân tại cơ sở hàng năm. Thông tin này sẽ được báo cáo thông qua trang thông tin điện tử AMR mỗi năm một lần (chi tiết trong Phụ lục B: Báo cáo về quần thể và dữ liệu thu thập về nuôi cấy hàng tháng).
2. Phương pháp vi khuẩn học và kháng sinh đồ (AST)
Phân lập, định danh và AST phải được thực hiện theo các tiêu chuẩn quốc tế được nêu trong tài liệu M100 của Viện Tiêu chuẩn Lâm sàng và Phòng xét nghiệm (Clinical and Laboratory Standards Institute - CLSI) (tài liệu được cập nhật hàng năm).
Thử nghiệm kháng sinh đồ cho các tác nhân gây bệnh cần được tiến hành theo một trong các phương pháp sau:
- Phương pháp khoanh giấy khuếch tán Kirby Bauer: kết quả được báo cáo là đường kính vòng ức chế.
- Phương pháp kháng sinh đồ tự động (ví dụ: Vitek, Phoenix, Microscan): kết quả được báo cáo là giá trị nồng độ ức chế tối thiểu (Minimum Inhibitory Concentration - MIC).
- Khuếch tán theo gradient nồng độ: kết quả được báo cáo là giá trị MIC.
Kết quả kháng sinh đồ đối với các tác nhân ưu tiên giám sát phải được báo cáo dưới dạng đường kính vòng ức chế hoặc là giá trị MIC. Trong trường hợp phòng xét nghiệm không thể chuyển kết quả đường kính vòng ức chế và giá trị MIC sang định dạng tệp tin WHONET thì có thể báo cáo kết quả là Nhạy cảm (S), Trung gian (I) hoặc Đề kháng (R), đồng thời Đơn vị AMR tiếp tục phối hợp với Phòng xét nghiệm để tìm cách khắc phục và báo cáo dữ liệu dưới dạng đường kính vòng ức chế và MIC.
3. Nhập dữ liệu vào WHONET
Tất cả các kết quả nuôi cấy sẽ được lưu trong cơ sở dữ liệu sẵn có của các phòng xét nghiệm. Các kết quả này nhanh chóng được gửi tới khoa lâm sàng theo quy trình của từng bệnh viện. Để Đơn vị AMR thực hiện được phân tích dữ liệu, các dữ liệu nuôi cấy dương tính và âm tính cần được lưu trữ trong cơ sở dữ liệu của phòng xét nghiệm. Các phòng xét nghiệm sẽ có hai lựa chọn để gửi dữ liệu nuôi cấy dương tính và nuôi cấy âm tính đến VNASS:
a) Phương pháp ưu tiên thực hiện: Nhập tất cả các kết quả nuôi cấy dương tính và âm tính vào WHONET và gửi tệp tin đó đến cổng thông tin điện tử AMR của Cục Quản lý Khám, chữa bệnh (kks.kcb.vn).
HOẶC
b) Nhập tất cả các kết quả nuôi cấy dương tính vào WHONET và gửi file dữ liệu hàng tháng đến cổng đến cổng thông tin điện tử AMR của Cục Quản lý Khám, chữa bệnh (kks.kcb.vn). Đồng thời, hàng tháng báo cáo tổng số mẫu bệnh phẩm nuôi cấy dương tính và âm tính của phòng xét nghiệm đến cổng thông tin điện tử như hướng dẫn tại Phụ lục B - Báo cáo về quần thể và thu thập dữ liệu nuôi cấy hàng tháng.
Các phòng xét nghiệm có thể nhập dữ liệu vào WHONET bất kỳ thời gian nào trong tháng; tuy nhiên nên nhập hàng ngày để bảo đảm gửi dữ liệu kịp thời và đầy đủ.
4. Dữ liệu phải báo cáo cho VNASS
Các mã phòng xét nghiệm theo WHONET sau đây sẽ được sử dụng cho 16 phòng xét nghiệm trong Hệ thống giám sát AMR:
Bảng 2: Các mã phòng xét nghiệm theo WHONET
|
Đơn vị/Phòng xét nghiệm |
Mã phòng, XN |
Đơn vị/Phòng xét nghiệm |
Mã phòng XN |
|
Bệnh viện Bạch Mai |
BMA |
Bệnh viện đa khoa Đà Nẵng |
DNG |
|
Bệnh viện Bệnh nhiệt đới trung ương |
CLI |
Bệnh viện đa khoa tỉnh Bình Định |
BID |
|
Bệnh viện Nhi Trung ương |
VCH |
Bệnh viện đa khoa tỉnh ĐakLak |
016 |
|
Bệnh viện Việt - Đức |
VD |
Bệnh viện đa khoa tỉnh Khánh Hòa |
KH |
|
Bệnh viện đa khoa Xanh Pôn |
123 |
Bệnh viện Chợ Rẫy |
CRH |
|
BV Hữu nghị Việt Tiệp |
H06 |
Bệnh viện Bệnh Nhiệt đới TP HCM |
HTD |
|
BV Việt Nam - Thụy Điển, Uông Bí |
UBI |
Bệnh viện Nhi Đồng 1 |
CH1 |
|
Bệnh viện Trung ương Huế |
HUE |
Bệnh viện đa khoa trung ương Cần Thơ |
WTH |
Các phòng xét nghiệm sẽ gửi tất cả các kết quả nuôi cấy vi khuẩn của các mẫu lấy từ các khoa lâm sàng. Các trường dữ liệu trong cấu hình phòng xét nghiệm chuẩn hóa theo WHONET được liệt kê trong Bảng 3. Thông tin trong mỗi trường dữ liệu cần được nhập và báo cáo đầy đủ cho mỗi phân lập cũng như trong toàn bộ file dữ liệu. Các trường dữ liệu bổ sung có thể được đưa thêm vào cấu hình phòng xét nghiệm WHONET tùy theo nhu cầu sử dụng của các phòng xét nghiệm.
Bảng 3: Các trường dữ liệu bắt buộc đối với cấu hình phòng xét nghiệm WHONET
|
Trường dữ liệu WHONET |
Định nghĩa |
Định dạng |
|
Institution Đơn vị |
Mã ID gồm ba ký tự cho bệnh viện nơi lấy bệnh phẩm |
Xem Bảng 2 |
|
Laboratory Phòng xét nghiệm |
Mã ID ba ký tự cho phòng xét nghiệm- nơi mẫu bệnh phẩm được làm xét nghiệm |
Xem Bảng 2 |
|
Patient_ID ID bệnh nhân |
Số hồ sơ bệnh án hoặc số nhận dạng duy nhất khác được gắn cho bệnh nhân trong quá trình đăng ký hoặc nhập viện. |
Số hoặc Chữ số |
|
Sex Giới tính |
Giới tính của bệnh nhân |
Nam, Nữ, hoặc Khác |
|
Date_Birth Ngày tháng năm sinh |
Ngày sinh của BN (bắt buộc đối với bệnh nhân ≤2 tuổi) |
DD/MM/YYYY |
|
Age Tuổi |
Tuổi của bệnh nhân, làm tròn xuống số nguyên gần nhất |
Tuổi (≥1 tuổi) Tháng (<1 tuổi, ≥1 tháng) Ngày (<1 tháng) |
|
Date_Admission Ngày vào viện |
Ngày bệnh nhân được nhập viện. |
DD/MM/YYYY |
|
Ward_Type Loại bệnh phòng |
Bệnh phòng nơi bệnh nhân nằm tại thời điểm lấy bệnh phẩm |
ICU (hồi sức tích cực), Nội trú không phải ICU, Ngoại trú. |
|
Department Khoa |
Tên khoa nơi bệnh nhân nằm tại thời điểm lấy bệnh phẩm |
Tùy từng đơn vị (ví dụ, khoa nhi, khoa tim mạch) |
|
Spec_Num Mã bệnh phẩm |
Mã duy nhất được gắn cho mỗi mẫu bệnh phẩm khi phòng xét nghiệm nhận mẫu |
Số hoặc Chữ số |
|
Spec_Date Ngày lấy bệnh phẩm |
Ngày bệnh nhân được lấy bệnh phẩm |
DD/MM/YYYY |
|
Spec_Type Loại bệnh phẩm |
Loại bệnh phẩm được lấy từ bệnh nhân |
VD: máu, nước tiểu, dịch hô hấp, dịch não tủy, dịch cơ thể vô trùng khác, phân, vết thương... |
|
Organism Tên tác nhân |
Gọi tên chi, và nếu có thể thì gọi đến tên loài tác nhân gây bệnh đã được phân lập. |
Định dạng chuẩn trong WHONET |
|
ASTa Kháng sinh đồa |
Kết quả kháng sinh đồ được thực hiện bằng phương pháp khoanh giấy, phương pháp tự động, hoặc khuếch tán gradient. |
Khuếch tán khoanh giấy: Đường kính vòng ức chế (mm) Kháng sinh đồ tự động: Giá trị MIC (µg/ml) Khuếch tán gradient: Giá trị MIC (µg/ml) |
a Lưu ý: trong trường hợp phòng xét nghiệm không thể cung cấp kết quả kháng sinh đồ dưới dạng đường kính vòng ức chế hay giá trị MIC thì có thể báo cáo kết quả kháng sinh đồ dưới dạng nhạy cảm (S), Trung gian (I) hoặc Đề kháng (R) đối với từng kháng sinh.
Đối với trường ngày/tháng/năm sinh: có thể nhập năm sinh nếu không có đủ thông tin ngày/tháng/năm sinh. Đối với trường ngày vào viện: khuyến khích nhưng không bắt buộc phải nhập và báo cáo thông tin này trong giai đoạn đầu triển khai thực hiện giám sát kháng kháng sinh.
5. Loại bỏ các dữ liệu trùng lặp
Sau khi Đơn vị AMR nhận được các tập tin WHONET, các số liệu trùng lặp của cùng một bệnh nhân sẽ được loại bỏ (lọc trùng). Việc lọc trùng dữ liệu sẽ được thực hiện cho mỗi giai đoạn giám sát và chỉ lấy kết quả đầu tiên để phân tích cho mỗi bệnh nhân theo loại mẫu bệnh phẩm và tác nhân gây bệnh được khảo sát. Nếu các kết quả nuôi cấy âm tính được nhập vào WHONET thì các mẫu nuôi cấy âm tính lặp lại cho cùng một loại mẫu bệnh phẩm của cùng một bệnh nhân cũng sẽ được lọc trùng.
Để đảm bảo có thể lọc trùng dữ liệu, các cơ sở phải bảo đảm rằng tất cả các kết quả nuôi cấy được gửi trong tệp tin WHONET tới Cục Quản lý Khám, chữa bệnh và đảm bảo rằng mỗi kết quả được gán với một thông tin nhận dạng bệnh nhân duy nhất hoặc là số hoặc là chữ số (tên trường dữ liệu WHONET là: "Patient_ID"). Thông thường, đây là số hồ sơ bệnh án do bệnh viện chỉ định (gán) trong quá trình đăng ký bệnh nhân. Nếu bệnh viện không có một hệ thống chuẩn hóa để gán số hồ sơ bệnh án (hoặc mã duy nhất nhận dạng bệnh nhân cần thông tin cho Đơn vị AMR và khi gửi tệp tin phải sử dụng họ tên bệnh nhân đầy đủ cho đến khi tìm ra giải pháp giải quyết vấn đề này).
6. Gửi dữ liệu đến Đơn vị AMR
a) Tần suất báo cáo
Các phòng xét nghiệm phải thực hiện thu thập và báo cáo dữ liệu đảm bảo chất lượng theo đúng thời hạn và yêu cầu báo cáo. Mỗi phòng xét nghiệm sẽ tổng hợp dữ liệu AMR (cả phương pháp khoanh giấy khuếch tán, tự động và E-test) của 1 tháng vào một tệp tin WHONET duy nhất và tải tệp tin này lên cổng thông tin điện tử bảo mật của Cục Quản lý Khám, chữa bệnh: kks.kcb.vn. Thời hạn gửi báo cáo: trước ngày mùng 10 của tháng sau (ví dụ, dữ liệu từ ngày 01/01/2019 đến ngày 31/01/2019 sẽ được báo cáo lên cổng thông tin kks.kcb.vn trước ngày 10/2/2019).
b) Định dạng tệp tin
Dữ liệu phải được gửi trong một tệp tin WHONET duy nhất, trong đó bao gồm cả kết quả AST theo phương pháp khoanh giấy khuếch tán và MIC. Hướng dẫn tạo một tệp tin WHONET tại Phụ lục C - Hướng dẫn cách tải một tệp tin WHONET lên cổng thông tin điện tử AMR: kks.kcb.vn. Mỗi tệp tin phải được đặt tên theo định dạng được chuẩn hóa bao gồm mã phòng xét nghiệm gồm ba ký tự, tháng (MM) và năm (YYYY). Ví dụ, dữ liệu tháng 1 năm 2018 của Bệnh viện Bạch Mai sẽ được đặt tên là BMH_012018. Đơn vị AMR phối hợp với các đối tác quốc tế và các chuyên gia vi sinh trong nước hỗ trợ kỹ thuật cho các phòng xét nghiệm chỉnh sửa cấu hình WHONET nhằm đạt được các tiêu chuẩn tối thiểu về báo cáo, tích hợp WHONET vào luồng dữ liệu phòng xét nghiệm và tổng hợp các tệp tin dữ liệu hàng tháng để gửi tới Đơn vị AMR.
c) Gửi đến cổng thông tin điện tử bảo mật: Hướng dẫn cách tải tệp tin dữ liệu đến cổng thông tin điện tử bảo mật AMR theo Phụ lục C.
CHƯƠNG 2: CÁC TÁC NHÂN ƯU TIÊN, BỆNH PHẨM VÀ AST ĐỂ PHÂN TÍCH DỮ LIỆU
Tác nhân gây bệnh và bệnh phẩm lâm sàng
Các phòng xét nghiệm sẽ gửi tất cả các kết quả nuôi cấy vi khuẩn của các mẫu bệnh phẩm thường quy được xét nghiệm theo yêu cầu của lâm sàng. Các dữ liệu sẽ được sử dụng ưu tiên cho mục đích phân tích và giám sát chất lượng, như được mô tả tại Bảng 4. Để đảm bảo chuẩn hóa và chất lượng của dữ liệu vi sinh được báo cáo cho Cục Quản lý Khám, chữa bệnh các yêu cầu tối thiểu về xét nghiệm AST và báo cáo đối với các vi khuẩn ưu tiên được mô tả trong Phụ lục A1, A2 và được dựa trên các hướng dẫn trong tài liệu CLSI M100:
Bảng 4: Các tác nhân gây bệnh và các mẫu bệnh phẩm ưu tiên giám sát
|
Bệnh phẩm |
Vi khuẩn ưu tiên giám sát |
|
Máu |
E. coli K. pneumonia A. baumannii S. aureus S. pneumonia Salmonella spp. |
|
Nước tiểu |
E. coli K. pneumoniae |
|
Phân |
Salmonella spp. Shigella spp |
|
Dịch niệu đạo và âm đạo |
N. gonorrhoeae |
|
Bệnh phẩm từ các vị trí vô trùng khác của cơ thể Dịch não tủy Dịch khớp Dịch khớp háng Dịch màng phổi Dịch màng ngoài tim Hoạt dịch Dịch màng bụng Mủ từ ổ áp xe Hạch bạch huyết |
Acinetobacter spp. Escherichia coli Enterococcus spp. Klebsiella spp. Pseudomonas spp. Staphylococcus aureus Streptococcus pneumoniae |
CHƯƠNG 3: CÁC TIÊU CHUẨN TRONG GIÁM SÁT VÀ BÁO CÁO
1. Các phòng xét nghiệm Vi sinh
a) Năng lực kỹ thuật
• Có đủ năng lực thực hiện việc lấy bệnh phẩm, nuôi cấy, định danh vi khuẩn và xét nghiệm kháng sinh đồ theo tiêu chuẩn của CLSI.
• Sẵn sàng tham gia đánh giá phòng xét nghiệm để nâng cao năng lực xét nghiệm và giám sát kháng kháng sinh.
b) Mua sắm vật tư phòng xét nghiệm và bảo trì thiết bị
• Đảm bảo quản lý lưu trữ thích hợp đối với tất cả các thuốc thử, sinh phẩm và vật tư cần thiết để đảm bảo các xét nghiệm nuôi cấy, định danh và kháng sinh đồ có thể được thực hiện vào mọi thời điểm.
• Tuân thủ và duy trì hồ sơ bảo trì và sửa chữa hoặc thay thế thiết bị một cách phù hợp khi cần thiết.
• Có kế hoạch dự phòng để dịch vụ xét nghiệm không bị gián đoạn do thiếu vật tư hoặc khi hỏng thiết bị. Nếu phòng xét nghiệm, tạm thời hoặc dài hạn không thể duy trì vật tư và thiết bị phù hợp để khắc phục việc gián đoạn dịch vụ xét nghiệm, cần thông báo cho Đơn vị AMR càng sớm càng tốt.
c) Thực hiện nội kiểm
• Thực hiện kiểm soát chất lượng (QC) đối với các loại môi trường, thuốc thử và kháng sinh với tần suất phù hợp theo tiêu chuẩn quốc tế do CLSI công bố hoặc tương đương và sử dụng các chủng tham chiếu tiêu chuẩn, chẳng hạn như ATCC (Đơn vị AMR sẽ hỗ trợ chủng tối thiểu 18 chủng chuẩn ATCC kèm theo hồ sơ chủng cho 16 phòng xét nghiệm thực hiện QC kháng sinh đồ).
• Ghi lại các kết quả QC và các biện pháp khắc phục đã được thực hiện; lưu trữ hồ sơ đầy đủ.
d) Ngoại kiểm
• Tham gia vào chương trình EQA hàng tháng để giám sát độ chính xác và độ tin cậy của các xét nghiệm định danh và kết quả kháng sinh đồ [trong giai đoạn triển khai ban đầu là tham gia vào chương trình ngoại kiểm UK-NEQAS (United Kingdom National External Quality Assessment Service - NEQAS)
• Tham gia vào công tác rà soát, đánh giá kết quả ngoại kiểm và thực hiện điều chỉnh khi kết quả ngoại kiểm không đạt với sự hỗ trợ của OUCRU, các chuyên gia vi sinh của Việt Nam và các đối tác quốc tế nếu cần.
đ) Lưu trữ và gửi một số chủng phân lập đặc biệt
• Các phòng xét nghiệm sẽ lưu trữ và gửi một số chủng phân lập đặc biệt về phương diện dịch tễ học hoặc vi sinh tới phòng xét nghiệm tham chiếu để thực hiện xét nghiệm khẳng định và xác định đặc điểm sinh học phân tử của kháng thuốc.
e) Quản lý dữ liệu
• Đảm bảo có đủ nhân viên và cơ sở vật chất phù hợp để thực hiện các hoạt động giám sát kháng kháng sinh.
• Đảm bảo nhân viên được đào tạo phù hợp về thu thập, phân tích và báo cáo dữ liệu kháng kháng sinh theo phương diện dịch tễ học, lâm sàng và xét nghiệm.
• Dành thời gian cho các nhân viên thực hiện nhiệm vụ nhập, đối chiếu và báo cáo dữ liệu giám sát một cách kịp thời, và đầy đủ dữ liệu, đảm bảo chất lượng cho Đơn vị AMR.
• Xây dựng phương pháp chia sẻ dữ liệu AMR với khoa Kiểm soát nhiễm khuẩn và các khoa lâm sàng ít nhất là hàng quý
• Xây dựng cách thức để thông tin với khoa Kiểm soát nhiễm khuẩn và các khoa lâm sàng khi phân lập được các tác nhân gây bệnh đòi hỏi các biện pháp dự phòng/cách ly (ví dụ: cách ly tiếp xúc).
• Viết các báo cáo riêng cho từng bệnh viện về các tác nhân gây bệnh và mô hình nhạy cảm kháng sinh ("bảng thống kê kháng sinh- cumulative antibiogram của bệnh viện") theo năm để chia sẻ với các khoa lâm sàng và các bác sĩ, giúp định hướng cho việc thực hành kê đơn dựa trên mô hình đề kháng kháng sinh tại đơn vị.
2. Đơn vị AMR
Để đảm bảo triển khai và điều phối thành công Hệ thống giám sát, Đơn vị AMR sẽ bao gồm các nhân sự chủ chốt của VAMS với các trách nhiệm quan trọng cần thiết để hỗ trợ VNASS trong các lĩnh vực sau:
a) Lãnh đạo có tính chiến lược
• Giám sát và điều phối hoạt động của Hệ thống giám sát quốc gia về kháng kháng sinh.
• Xây dựng các phương pháp giám sát và các yêu cầu về báo cáo cho các phòng xét nghiệm tham gia trong Hệ thống giám sát.
• Xác định chiến lược cần thiết để tham gia GLASS thành công
• Đại diện cho VNASS trong các cuộc họp, hội nghị, các cuộc họp của các bên liên quan và các diễn đàn quốc gia và quốc tế có liên quan khác.
• Phối hợp với các đơn vị khác trong Bộ Y tế để thực hiện giám sát kháng kháng sinh theo phương pháp tiếp cận "một sức khỏe" (One Health)
• Lựa chọn và tạo điều kiện thuận lợi cho các cơ sở giám sát trọng điểm tham gia hoạt động giám sát kháng kháng sinh.
• Huy động các bên liên quan về xét nghiệm tại các Bệnh viện tham gia hỗ trợ giám sát kháng kháng sinh cho các bệnh viện.
• Đóng vai trò kết nối giữa lãnh đạo Bộ Y tế và các đơn vị thực hiện giám sát.
b) Đảm bảo chất lượng
• Xây dựng và phổ biến các hướng dẫn chuẩn, quy trình, công cụ giám sát AMR trên cơ sở tham vấn với các đối tác quốc tế và nhóm kỹ thuật khi cần thiết.
• Xác nhận việc tuân thủ chương trình nội kiểm và ngoại kiểm của các phòng xét nghiệm trong hệ thống giám sát.
• Xác nhận sự sẵn có của vật tư, hóa chất, sinh phẩm có chất lượng tại các phòng xét nghiệm trong hệ thống giám sát
• Đáp ứng nhu cầu về đào tạo và hỗ trợ kỹ thuật của các phòng xét nghiệm trong Hệ thống giám sát khi cần thiết.
c) Quản lý dữ liệu và báo cáo
• Đảm bảo tất cả các phòng xét nghiệm đều có thể truy cập vào phần mềm WHONET để báo cáo dữ liệu giám sát và cập nhật WHONET ít nhất là hàng năm.
• Đảm bảo duy trì cổng thông tin điện tử AMR để gửi dữ liệu, bao gồm đảm bảo sự toàn vẹn và bảo mật dữ liệu.
• Giám sát việc gửi tệp tin WHONET hàng tháng của phòng xét nghiệm đúng thời hạn và đầy đủ dữ liệu.
• Thực hiện kiểm tra định kỳ chất lượng dữ liệu của các tệp tin WHONET: về tuân thủ các hướng dẫn của CLSI, tuân thủ các quy trình AMR, tính hợp lý về vi khuẩn học và sự phù hợp trong phiên giải kết quả kháng sinh đồ theo kích thước vòng ức chế và MIC.
• Kịp thời phản hồi cho phòng xét nghiệm các sai sót về chất lượng dữ liệu, đồng thời thảo luận về cách thức khắc phục.
• Hỗ trợ kỹ thuật từ xa hoặc tại chỗ để trợ giúp các phòng xét nghiệm tích hợp WHONET trong quy trình quản lý dữ liệu và tối ưu hóa việc thu thập và báo cáo dữ liệu.
• Báo cáo dữ liệu giám sát AMR tổng hợp hàng năm cho các phòng xét nghiệm thuộc hệ thống giám sát và các bên liên quan, đồng thời bảo đảm tính bảo mật thông tin về dữ liệu và nguồn gốc dữ liệu, loại bỏ mọi thông tin nhận dạng bệnh viện khỏi bộ dữ liệu tổng hợp.
• Tổng hợp và gửi dữ liệu giám sát AMR tổng hợp hàng năm cho GLASS.
• Cung cấp dữ liệu đã phiên giải để sử dụng trong xây dựng chính sách và hướng dẫn.
CHƯƠNG IV: GIÁM SÁT VÀ ĐÁNH GIÁ
Giám sát VNASS sẽ bắt đầu thực hiện vào năm 2019. Giám sát thường xuyên việc gửi dữ liệu và chất lượng dữ liệu sẽ do Đơn vị AMR thực hiện với sự hỗ trợ của các chuyên gia vi sinh trong nước và các đối tác quốc tế. Các chỉ số về chất lượng dữ liệu và tính đầy đủ của dữ liệu sẽ được Đơn vị AMR hoàn thành hàng tháng với phản hồi được hiển thị đối với mỗi phòng xét nghiệm trên cổng thông tin điện tử AMR. Cũng có thể có phản hồi, thu thập thông tin và hỗ trợ kỹ thuật bổ sung giữa Đơn vị AMR và phòng xét nghiệm thông qua thảo luận qua điện thoại hoặc làm việc trực tiếp tại cơ sở khi cần thiết.
Khi công bố các bài báo khoa học liên quan đến dữ liệu bệnh viện: cần được sự đồng ý/cho phép của bệnh viện và đưa tên các cán bộ tham gia chương trình giám sát làm đồng tác giả.
Các chỉ số về dữ liệu sẽ bao gồm nhưng không giới hạn các nội dung sau:
1. Chất lượng và tính đầy đủ của dữ liệu:
- Phần trăm số lần gửi dữ liệu đúng thời hạn, theo phòng xét nghiệm.
- Phần trăm các biến bắt buộc có trong tệp tin dữ liệu WHONET mô tả trong Bảng 3.
- Tính đầy đủ của các biến dữ liệu có trong mỗi tệp tin dữ liệu WHONET đã gửi.
- Phần trăm các cơ sở tuân thủ theo hướng dẫn của CLSI về các tác nhân gây bệnh ưu tiên, dựa trên các yêu cầu được liệt kê tại Phụ lục A1, A2. Giám sát này sẽ bao gồm:
o Danh mục kháng sinh thử nghiệm (antibiotic panel) phù hợp theo mẫu bệnh phẩm và nguồn mẫu bệnh phẩm.
o Các chú thích phù hợp kèm theo.
o Các kết quả AST mâu thuẫn hoặc không hợp lý dựa trên kiểm tra dữ liệu.
2. Chỉ số chất lượng phòng xét nghiệm:
- Phần trăm số phòng xét nghiệm thực hiện nội kiểm ít nhất hàng tuần.
- Phần trăm số phòng xét nghiệm ghi lại hành động khắc phục khi QC không đạt
- Phần trăm số phòng xét nghiệm tham gia EQA hàng tháng.
- Phần trăm số phòng xét nghiệm có kết quả EQA đạt hàng tháng
- Phần trăm số phòng xét nghiệm ghi lại hành động khắc phục khi EQA không đạt.
Năm 2019, Bộ Y tế sẽ thực hiện đánh giá Hệ thống giám sát quốc gia về kháng kháng sinh. Nhóm đánh giá do Bộ Y tế thành lập, bao gồm đại diện Đơn vị AMR, các chuyên gia vi sinh trong nước và các đối tác quốc tế. Đánh giá sẽ dựa vào các mục tiêu và cấu trúc Hệ thống giám sát được mô tả trong tài liệu này. Thành viên trong Nhóm đánh giá sẽ làm việc cùng nhau để thiết kế đánh giá nhằm mô tả và cải thiện hiệu suất thực hiện chương trình. Tài liệu sử dụng trong đánh giá Hệ thống giám sát là khung kế hoạch đánh giá chương trình đã được xây dựng bởi CDC và hiệu chỉnh cho phù hợp với Việt Nam (Bản Hướng dẫn cập nhật đánh giá Hệ thống giám sát sức khỏe công cộng, CDC 1999). Các kết quả đánh giá sẽ được Đơn vị AMR báo cáo và phổ biến theo định dạng được thống nhất. Kết quả này sẽ được sử dụng để điều chỉnh Tài liệu "Hướng dẫn thực hiện Giám sát quốc gia về kháng kháng sinh" trước khi mở rộng Hệ thống giám sát.
DANH MỤC KHÁNG SINH THỬ NGHIỆM TỐI THIỂU CHO CÁC TÁC NHÂN GÂY BỆNH ƯU TIÊN
Danh mục kháng sinh thử nghiệm cho 8 tác nhân gây bệnh được liệt kê trong bảng dưới đây là các yêu cầu xét nghiệm và báo cáo tối thiểu đối với các phòng xét nghiệm khi tham gia mạng lưới giám sát kháng kháng sinh.
Ngoài ra, bệnh viện cần giám sát và báo cáo thêm 5 loại vi khuẩn phổ biến tại bệnh viện trong trường hợp 10 vi khuẩn phổ biến của bệnh viện không bao gồm 8 vi khuẩn trong danh sách của bảng dưới (VD: Steno/máu; Suit/dịch não tủy or máu, whitmore,...)
|
Vi khuẩn |
Kháng sinh được lựa chọn làm kháng sinh đồ |
|
Escherichia coli |
Co-trimoxazole Ciprofloxacin hoặc levofloxacin Ceftriaxone hoặc cefotaxime và ceftazidime Cefepime Imipenem, meropenem, ertapenem hoặc doripenem Colistin Ampicillin |
|
Klebsiella pneumoniae |
Co-trimoxazole Ciprofloxacin hoặc levofloxacin Ceftriaxone hoặc cefotaxime và ceftazidime Cefepime Imipenem, meropenem, ertapenem hoặc doripenem Colistin |
|
Acinetobacter baumannii |
Tigecycline hoặc minocycline Gentamicin và/hoặc amikacin Imipenem, meropenem, hoặc doripenem Colistin |
|
Staphylococcus aureus |
Cefoxitin |
|
Streptococcus pneumoniae |
Oxacillin, Penicillin G Co-trimoxazole Ceftriaxone hoặc cefotaxime |
|
Salmonella spp. |
Ciprofloxacin hoặc levofloxacin Ceftriaxone hoặc cefotaxime và ceftazidime Imipenem, meropenem, ertapenem hoặc doripenem |
|
Shigella spp. |
Ciprofloxacin và levofloxacin Ceftriaxone hoặc cefotaxime và ceftazidime Azithromycin |
|
Neisseria gonorrhea |
Cefixime, Ceftriaxone Spectinomycin Ciprofloxacin |
DANH MỤC KHÁNG SINH THỬ NGHIỆM CHO CÁC TÁC NHÂN GÂY BỆNH ƯU TIÊN
(khuyến khích các phòng xét nghiệm tuân thủ)
Danh mục kháng sinh thử nghiệm cho các tác nhân gây bệnh được liệt kê trong bảng dưới đây là các yêu cầu xét nghiệm và báo cáo khuyến khích các phòng xét nghiệm tuân thủ khi tham gia vào mạng lưới giám sát kháng kháng sinh.
Danh sách được xây dựng dựa trên tài liệu M100, Bảng 1A và 1B của CLSI. Các phòng xét nghiệm có thể tiến hành đặt/thử nghiệm thêm kháng sinh khác tùy theo chính sách của bệnh viện. Trong trường hợp phòng xét nghiệm gặp khó khăn khi triển khai thực hiện theo biểu mẫu kháng sinh này hoặc khi muốn thảo luận về sự thay thế kháng sinh trong biểu mẫu, phòng xét nghiệm cần liên hệ với Đơn vị AMR.
Các phòng xét nghiệm phải tuân thủ tất cả các hướng dẫn hiện hành của CLSI đối với xét nghiệm và báo cáo kháng sinh của tài liệu M100, đặc biệt là các chú thích của Bảng 1A và các nhận xét chung ở cuối mỗi phần của các Bảng 2A, 2B-1, 2B-2, 2C, 2D và 2G. Một số chú giải và nhận xét đã được đưa vào các bảng dưới đây.
Các phòng xét nghiệm sử dụng các hệ thống kháng sinh đồ tự động cũng phải tuân theo các hạn chế đề cập trong bản hướng dẫn sử dụng của từng bộ mẫu chuẩn đang được sử dụng. Đối với các phòng xét nghiệm sử dụng hệ thống Vitek thì họ được khuyến cáo sử dụng các bộ mẫu chuẩn GN74, GP67 và GP74 (cho Strep pneumoniae). Đối với các phòng xét nghiệm sử dụng hệ thống Phoenix thì họ được khuyến cáo sử dụng các bộ mẫu chuẩn NMIC-121, -123, hoặc -124; PMIC-100, -101 hoặc -102; và SMIC-101.
|
Các tác nhân gây bệnh được giám sát |
Nhóm kháng sinh |
Kháng sinh được giám sát |
|
GRAM ÂM |
||
|
Escherichia coli, Klebsiella pneumoniae |
Phối hợp với chất ức chế beta-lactamase |
Amoxicillin-clavulanate hoặc Ampicillin-sulbactam hoặc Piperacillin-tazobactam (chọn một hoặc nhiều hơn). |
|
Cephalosporin thế hệ 1 |
Cefazolin1 |
|
|
Cephalosporin thế hệ 3 |
Ceftriaxone hoặc Cefotaxime (chọn một hoặc nhiều hơn). |
|
|
Cephalosporin thế hệ 4 |
Cefepime |
|
|
Cephamycin |
Cefoxitin |
|
|
Carbapenem |
Imipenem hoặc Meropenem (chọn một hoặc nhiều hơn) |
|
|
Aminoglycoside |
Gentamicin và Tobramycin và Amikacin |
|
|
Fluoroquinolone |
Ciprofloxacin hoặc Levofloxacin (chọn một hoặc nhiều hơn)1 |
|
|
Nitrofuran |
Nitrofurantoin (chỉ cho các phân lập nước tiểu) |
|
|
Thuốc đối kháng con đường Folate |
Trimethoprim-Sulfamethoxazole (hay còn gọi là Co-trimoxazole) |
|
|
Lipopeptide |
Colistin2 hoặc Polymyxin B2 (chọn một hoặc nhiều hơn, chỉ có phương pháp BMD)1 |
|
|
Salmonella spp1 và Shigella spp3 |
Penicillin |
Ampicillin |
|
Cephalosporin thế hệ 3 |
Ceftriaxone hoặc Cefotaxime (chỉ xét nghiệm cho các phân lập từ máu và CSF, không xét nghiệm cho phân lập từ bệnh phẩm là phân) (chọn một hoặc nhiều hơn). |
|
|
Fluoroquinolone |
Ciprofloxacin hoặc Levofloxacin (chọn một hoặc nhiều hơn) |
|
|
Thuốc đối kháng con đường Folate |
TMP/SMX (hay còn gọi là Co-trimoxazole) |
|
|
Phenicol |
Chloramphenicol6 |
|
|
Pseudomonas aeruginosa |
Phối hợp với chất ức chế beta-lactamase |
Piperacillin/Tazobactam |
|
Cephalosporin thế hệ 3 |
Ceftazidime |
|
|
Cephalosporin thế hệ 4 |
Cefepime |
|
|
Carbapenem |
Imipenem or Meropenem (chọn một hoặc nhiều hơn) |
|
|
Monobactam |
Aztreonam |
|
|
Aminoglycoside |
Gentamicin và Tobramycin và Amikacin |
|
|
Fluoroquinolone |
Ciprofloxacin hoặc Levofloxacin (chọn một hoặc nhiều hơn)1 |
|
|
Lipopeptide |
Colistin2 hoặc Polymyxin B2 (chọn một hoặc nhiều hơn, chỉ áp dụng cho phương pháp BMD) |
|
|
Acinetobacter baumannii-calcoaceticus complex |
Phối hợp với chất ức chế beta-lactamase |
Ampicillin-sulbactam hoặc Piperacillin-tazobactam (chọn một hoặc nhiều hơn). |
|
Cephalosporin thế hệ 3 |
Ceftazidime và Cefotaxime hoặc Ceftriaxone (chọn một hoặc nhiều hơn). |
|
|
Cephalosporin thế hệ 4 |
Cefepime |
|
|
Carbapenem |
Imipenem hoặc Meropenem |
|
|
Aminoglycosides |
Gentamicin và Tobramycin và Amikacin |
|
|
Fluoroquinolones |
Ciprofloxacin1 hoặc Levofloxacin1 (chọn một hoặc nhiều hơn). |
|
|
Tetracyclines |
Tetracycline1 (chỉ báo cáo đối với phân lập nước tiểu). Doxycycline1 hoặc Minocycline1,4 (chọn một hoặc nhiều hơn). |
|
|
Thuốc đối kháng con đường Folate |
TMP/SMX (hay còn gọi là Co-trimoxazole) |
|
|
Lipopeptide |
Colistin2, Polymyxin B2 (chọn một hoặc nhiều hơn, chỉ có phương pháp BMD) |
|
|
GRAM DƯƠNG |
||
|
Staphylococcus aureus |
Cephamycin |
Cefoxitin2 (chỉ có thể thay thế bằng Oxacillin nếu sử dụng phương pháp MIC) |
|
Macrolide |
Erythromycin hoặc clarithromycin hoặc azithromycin (chọn một hoặc nhiều hơn)1,3 |
|
|
Lincosamide |
Clindamycin1,6 |
|
|
|
Thuốc đối kháng con đường Folate |
TMP/SMX (hay còn gọi là Co-trimoxazole) |
|
Glycopeptide |
Vancomycin (chỉ cho P. pháp MIC)4. |
|
|
Oxazolidinone |
Linezolid |
|
|
Tetracycline |
Tetracycline1,4 hoặc Doxycycline1,4 hoặc Minocycline1,4,6 (chọn một hoặc nhiều hơn) |
|
|
Ansamycin |
Rifampin5 (chỉ để điều trị phối hợp) |
|
|
Aminoglycoside |
Gentamicin (chỉ để điều trị phối hợp)6 |
|
|
Fluoroquinolone |
Ciprofloxacin1 hoặc Levofloxacin1 hoặc Moxifloxacin1 (chọn một hoặc nhiều hơn). |
|
|
Nitrofuran |
Nitrofurantoin (chỉ cho các phân lập từ nước tiểu) |
|
|
Enterococcus faecalis &E.faecium7 |
Penicillin |
Penicillin8 và Ampicillin9 |
|
Glycopeptide |
Vancomycin |
|
|
Oxazolidinone |
Linezolid |
|
|
Nitrofuran |
Nitrofurantoin (chỉ cho các phân lập từ nước tiểu). |
|
|
Streptococcus pneumoniae* *Chỉ các phân lập từ các vị trí vô trùng: máu, dịch não tủy, dịch màng phổi, dịch màng ngoài tim |
Penicillin |
Sàng lọc10 bằng khoan giấy Oxacillin (1ug) và/hoặc Penicillin (chỉ với phương pháp MIC)11 |
|
Cephalosporin thế hệ 3 |
Cefotaxime13 (chỉ với phương pháp MIC) hoặc Ceftriaxone13 (chỉ với phương pháp MIC) (chọn một hoặc nhiều hơn). |
|
|
Carbapenems |
Meropenem13 (chỉ với phương pháp MIC). |
|
|
Fluoroquinolones |
Levofloxacin1 (không cho phân lập từ CSF). |
|
|
Tetracycline |
Tetracycline1 (không cho phân lập từ CSF). |
|
|
Thuốc đối kháng con đường Folate |
TMP/SMX (hay còn gọi là Co-trimoxazole). |
|
|
Glycopeptide |
Vancomycin |
|
________________________
1 CẢNH BÁO: Các kháng sinh sau đây không được báo cáo thường quy cho vi khuẩn phân lập từ dịch não tủy (CSF): cephalosporin thế hệ 1 và thế hệ 2 và cephamycins, Clindamycin, Macrolides (ví dụ: Erythromycin, Azithromycin), Tetracycline, Fluoroquinolones, các kháng sinh chỉ dùng đường uống. Đây không phải là thuốc được lựa chọn và có thể không hiệu quả trong điều trị nhiễm trùng CSF.
2 Chỉ phải làm xét nghiệm Colistin/Polymyxin B đối với các phân lập kháng carbapenem. Gửi một mẫu cấy chuyển của tất cả các phân lập loại này đến một phòng thí nghiệm tham chiếu để xét nghiệm xác định hoặc xét nghiệm khẳng định về xét nghiệm đặc điểm phân tử. Phương pháp duy nhất được chấp thuận để xét nghiệm là MIC bằng pha loãng vi lượng canh thang. Không nên sử dụng phương pháp khuếch tán khoanh giấy kháng sinh và khuếch tán gradient.
3 CẢNH BÁO: Đối với Salmonella spp. và Shigella spp., aminoglycosides, cephalosporin thế hệ 1 và thế hệ 2 và cephamycins có thể hiệu quả ở in vitro, nhưng không hiệu quả trên lâm sàng và không được báo cáo là nhạy cảm.
4 Những sinh vật nhạy cảm với tetracycline khi xét nghiệm cũng nhạy cảm với doxycycline và minocycline và có thể được báo cáo là nhạy cảm mà không cần xét nghiệm thêm, với bất kể loại bệnh phẩm nào. Tuy nhiên, các sinh vật có kết quả là trung gian hoặc đề kháng với tetracycline có thể nhạy cảm với doxycycline và/hoặc minocycline và phải xét nghiệm với từng loại thuốc cụ thể để xác định kết quả.
5 Cefoxitin được xét nghiệm như một chất thay thế cho oxacillin. Xét nghiệm khoanh giấy kháng sinh Oxacillin không đáng tin cậy đối với Staph aureus (tụ cầu vàng). Các phân lập có kết quả xét nghiệm kháng sinh đồ đề kháng với cefoxitin bằng phương pháp khuếch tán khoanh giấy kháng sinh, cefoxitin bằng phương pháp MIC hoặc oxacillin bằng phương pháp MIC phải được báo cáo là kháng oxacillin. Các kết quả có thể được áp dụng đối với các penicilinin có penicillinase ổn định (oxacillin, methicillin, nafcillin, cloxacillin, dicloxacillin). Staphylococci (cầu khuẩn) kháng cefoxitin kháng với tất cả các thuốc beta-lactam hiện có trừ ceftaroline. Do đó, không khuyến cáo làm kháng sinh đồ với các thuốc beta-lactam khác.
6 Một số thuốc không được báo cáo một cách thường quy cho các vi sinh vật được phân lập từ đường tiết niệu: Macrolides, Lincosamides, Minocycline, Chloramphenicol.
7 Nếu không thực hiện được phương pháp MIC thì không làm kháng sinh đồ với vancomycin. Không yêu cầu làm kháng sinh đồ Vancomycin đối với tất cả các phân lập S.aureus nếu hiện tại đây không phải là công việc thường quy của phòng xét nghiệm. Gửi bất kỳ phân lập S.aureus nào đó mà kết quả kháng sinh đồ vancomycin theo phương pháp MIC > 8ug/ml đến một phòng xét nghiệm chuẩn thức.
8 Không nên dùng một mình Rifampin để điều trị
9 Đối với staphylococci mà có kết quả kháng sinh đồ nhạy cảm thì chỉ nên dùng aminoglycosid để điều trị bệnh nhân kết hợp với các thuốc có hoạt tính khác cũng có kết quả kháng sinh đồ nhạy cảm.
10 CẢNH BÁO: Đối với Enterococcus spp. thì Cephalosporin, aminoglycosid (trừ kết quả kháng sinh đồ đề kháng mức cao), clindamycin và co-trimoxazol có thể có hoạt tính ở in vitro, nhưng không hiệu quả trên lâm sàng và không được báo cáo là nhạy cảm.
11 Enterococci (các cầu khuẩn đường ruột) nhạy cảm với penicillin thì có thể dự đoán là nhạy cảm với ampicillin, amoxicillin, ampicillin-sulbactam, amoxicillin-clavulanate, piperacillin và piperacillin-tazobactam đối với enterococci không sinh beta-lactamase. Tuy nhiên, enterococci nhạy cảm với ampicillin thì lại không thể giả định rằng là nó sẽ nhạy cảm với penicillin.
12 Đối với Enterococcus spp, kết quả kháng sinh đồ nhạy cảm với ampicillin nên được sử dụng để dự đoán hoạt tính của amoxicillin.
13 Các phân lập Pneumococcus (phế cầu) có kích thước vòng vô khuẩn của oxacillin ≥ 20mm là nhạy cảm với penicillin. Đối với các phân lập có kích thước vòng vô khuẩn của oxacillin ≤ 19mm thì không báo cáo là kháng penicillin mà không thực hiện MIC penicillin. Phải xác định MIC của penicillin và cefotaxime, ceftriaxone, hoặc meropenem của những phân lập này bởi vì kích thước vòng vô khuẩn ≤ 19mm có ở cả các chủng kháng, trung gian, và chắc chắn nhạy cảm với penicillin.
14 Đối với các phân lập từ CSF, chỉ báo cáo phiên giải cho viêm màng não. Đối với các phân lập khác, báo cáo phiên giải cho cả viêm màng não và không viêm màng não.
BÁO CÁO VỀ QUẦN THỂ VÀ THU THẬP DỮ LIỆU NUÔI CẤY HÀNG THÁNG
Dữ liệu sau đây sẽ được nhập vào phần Nhập liệu (Data Entry) của cổng thông tin điện tử AMR: kks.kcb.vn; chi tiết yêu cầu những dữ liệu cho mục đích cung cấp thông tin sẽ có ở Phụ lục này. Các phòng xét nghiệm sẽ nhận được những hướng dẫn bổ sung về cách gửi dữ liệu này đến cổng thông tin điện tử.
Báo cáo hàng năm về dữ liệu quần thể bệnh nhân
• Dữ liệu sẽ được báo cáo mỗi năm một lần và được gửi trước ngày 31 tháng 1 của năm sau (ví dụ, dữ liệu năm 2019 phải được báo cáo trước ngày 31/01/2020).
- Năm báo cáo (ví dụ, "2019")
- Số giường bệnh của bệnh viện trong năm báo cáo
- Tổng số bệnh nhân nội trú trong năm báo cáo
- Tổng số bệnh nhân ngoại trú trong năm báo cáo
Báo cáo dữ liệu nuôi cấy hàng tháng
• Chỉ bắt buộc đối với các phòng xét nghiệm không báo cáo dữ liệu nuôi cấy âm tính hàng tháng trong tệp tin dữ liệu WHONET.
• Đối với từng loại bệnh phẩm: báo cáo tổng số nuôi cấy dương tính và tổng số nuôi cấy âm tính hàng tháng.
• Thời hạn gửi báo cáo: trước ngày mùng 10 của tháng sau (ví dụ, dữ liệu từ ngày 01/01/2019 đến ngày 31/01/2019 sẽ được báo cáo lên cổng thông tin kks.kcb.vn trước ngày 10/2/2019).
|
Bệnh phẩm |
Vi khuẩn ưu tiên cho việc giám sát |
|
Máu |
E. coli K. pneumonia A. baumannii S. aureus S. pneumonia Salmonella spp. |
|
Nước tiểu |
E. coli K. pneumoniae |
|
Phân |
Salmonella spp. Shigella spp |
|
Dịch niệu đạo và âm đạo |
N. gonorrhoeae |
|
Bệnh phẩm từ vị trí vô trùng khác của cơ thể Dịch não tủy Dịch khớp Dịch khớp háng Dịch màng phổi Dịch màng ngoài tim Hoạt dịch Dịch màng bụng Mủ từ ổ áp xe Hạch bạch huyết |
Acinetobacter spp. Escherichia coli Enterococcus spp. Klebsiella spp. Pseudomonas spp. Staphylococcus aureus Streptococcus pneumoniae |
HƯỚNG DẪN CÁCH TẢI MỘT TỆP TIN WHONET LÊN CỔNG THÔNG TIN ĐIỆN TỬ AMR: kks.kcb.vn
1. Giới thiệu
Tài liệu này sử dụng để hướng dẫn các phòng xét nghiệm gửi dữ liệu vi sinh (theo định dạng WHONET) đến cổng thông tin điện tử AMR của cục quản lý khám chữa bệnh - Bộ Y tế. Tài liệu bao gồm hướng dẫn chi tiết các bước gửi tệp dữ liệu WHONET và số liệu tổng số mẫu xét nghiệm hàng tháng và xem các phản hồi từ nhóm chuyên gia về tệp dữ liệu.
2. Đăng nhập
Username: Sẽ được cung cấp đến từng phòng xét nghiệm
Password: Sẽ được cung cấp đến từng phòng xét nghiệm
Người sử dụng: Nhân viên phòng xét nghiệm vi sinh người sẽ trực tiếp nộp báo cáo lên
Trình duyệt web: Chrome, Firefox
Địa chỉ báo cáo: http://kks.kcb.vn

Nhập tên tài khoản và mật khẩu.
3. Bảng hiển thị
Sau khi đăng nhập màn hình hiển thị đầu tiên sẽ hiện ra
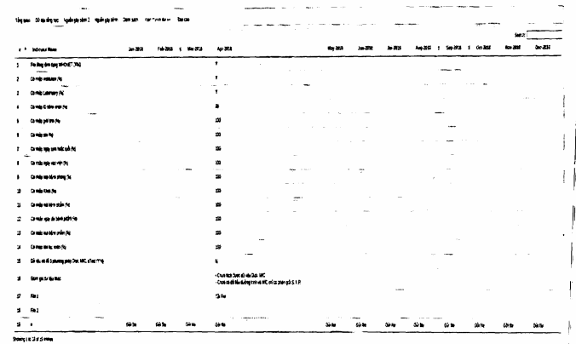
Màn hình hiển thị sẽ thể hiện những thông tin về mức độ hoàn thành của dữ liệu theo các tháng, và hiển thị các đánh giá, phản hồi từ nhóm xem xét dữ liệu.
4. Nhập và gửi báo cáo
Bước 1: Nhấn vào nút "Gửi file" ở dưới màn hình
Bước 2: Chọn "Biểu nhập" và thời điểm

Bước 3: Gửi file dữ liệu bằng cách nhấn vào nút "" và chọn file cần gửi
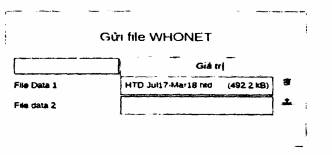
Bước 4: Đợi đến khi gửi file thành công và ô "file" chuyển sang màu xanh.

Bước 5: Nhập số mẫu xét nghiệm theo tháng (Chỉ yêu cầu với các phòng xét nghiệm không có dữ liệu kết quả xét nghiệm âm tính trong file WHONET)
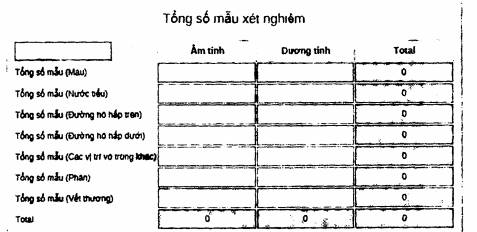
Bước 6: Nhấn vào "Hoàn thành"

(Không có nội dung)
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
(Không có nội dung)
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
-
Ban hành: {{m.News_Dates_Date}} Hiệu lực: {{m.News_EffectDate_Date}} Tình trạng: {{m.TinhTrang}} Cập nhật: {{m.Email_SendDate_Date}} Ban hành: {{m.News_Dates_Date}}Hiệu lực: {{m.News_EffectDate_Date}}Tình trạng: {{m.TinhTrang}}Cập nhật: {{m.Email_SendDate_Date}}
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
-
Ban hành: {{m.News_Dates_Date}} Hiệu lực: {{m.News_EffectDate_Date}} Tình trạng: {{m.TinhTrang}} Cập nhật: {{m.Email_SendDate_Date}} Ban hành: {{m.News_Dates_Date}}Hiệu lực: {{m.News_EffectDate_Date}}Tình trạng: {{m.TinhTrang}}Cập nhật: {{m.Email_SendDate_Date}}
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây
Vì chưa Đăng Nhập nên Bạn chỉ xem được Thuộc tính của Văn bản. Bạn chưa xem được Hiệu lực của Văn bản, Văn bản Liên quan, Văn bản thay thế, Văn bản gốc, Văn bản tiếng Anh,...
Nếu chưa có Tài khoản, mời Bạn Đăng ký Tài khoản tại đây