Thông tư 01/2018/TT-BYT
-

- 04 chính sách y tế - dược chính thức có hiệu lực từ tháng 6/2018
- 08:19, 21/05/2018
- Bắt đầu từ tháng 6/2018, nhiều chính sách quan trọng sẽ chính thức có hiệu lực. Nổi bật là các chính sách liên quan đến lĩnh vực Y tế - Dược được đề cập tại bài viết dưới đây.
-

- Điểm mới về các dấu hiệu lưu ý và khuyến cáo được ghi trên thuốc
- 10:32, 14/05/2018
- Kể từ ngày 01/6/2018, Thông tư 01/2018/TT-BYT của Bộ Y tế chính thức có hiệu lực thi hành; trong đó, đáng chú ý là bổ sung thêm quy định về các dấu hiệu cần lưu ý và khuyến cáo khi dùng thuốc.
-
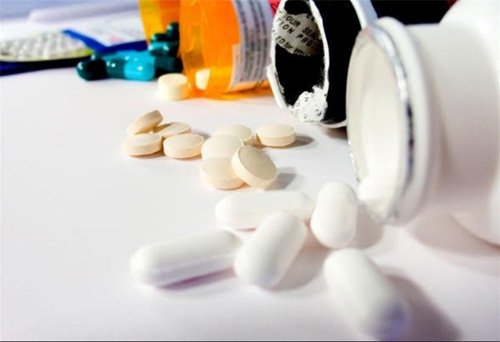
- Các dấu hiệu lưu ý và khuyến cáo khi dùng thuốc
- 08:37, 13/05/2018
- Đây là nội dung đáng chú ý tại Thông tư 01/2018/TT-BYT về quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc được ban hành ngày 18/01/2018.
-

- Những điểm mới quy định ghi nhãn thuốc, nguyên liệu làm thuốc
- 08:19, 13/05/2018
- Cục Quản lý Dược (Bộ Y tế) cho biết, Bộ Y tế đã ban hành Thông tư số 01/2018/TT-BYT ngày 18/01/2018 của Bộ trưởng Bộ Y tế quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc thay thế Thông tư số 06/2016/TT-BYT ngày 08/03/2016 của Bộ Y tế về nội dung này trước đó.
-
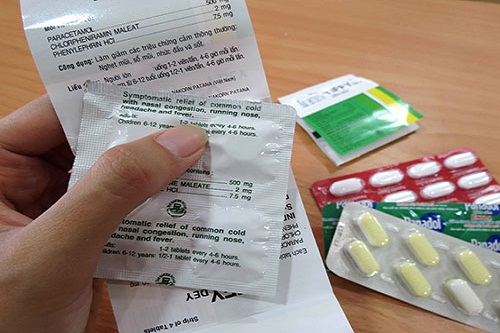
- Nhãn thuốc phải hướng dẫn cách xử lý khi dùng thuốc quá liều
- 08:25, 24/01/2018
- Bộ Y tế vừa ban hành Thông tư 01/2018/TT-BYT quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc. Thông tư nêu rõ, các triệu chứng, biểu hiện và hướng dẫn xử trí khi sử dụng thuốc quá liều cần được thông tin đầy đủ trong hướng dẫn sử dụng thuốc.
-

- Đã có cách ghi nhãn thuốc mới nhất áp dụng từ 01/6/2018
- 08:17, 24/01/2018
- Ngày 18/01/2018, Bộ Y tế đã ban hành Thông tư 01/2018/TT-BYT quy định về ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc.
-

- Quy định mới về ghi nhãn thuốc, nguyên liệu làm thuốc
- 08:31, 22/01/2018
- Bộ Y tế vừa ban hành Thông tư số 01/2018/TT-BYT quy định ghi nhãn thuốc, nguyên liệu làm thuốc và tờ hướng dẫn sử dụng thuốc.
Xem nhiều nhất
 Cách tính hưởng chính sách đối với người nghỉ hưu trước tuổi theo Thông tư 01/2025
Cách tính hưởng chính sách đối với người nghỉ hưu trước tuổi theo Thông tư 01/2025 Dưới đây là cách tính hưởng chính sách đối với người nghỉ hưu trước tuổi theo Thông tư 01/2025/TT-BNV.
- Chương trình khung cập nhật kiến thức hành nghề dịch vụ làm thủ tục về thuế năm 2025
- Đối tượng được điều chỉnh tiền lương và thu nhập tháng đã đóng BHXH theo Thông tư 01/2025
- Hành vi ép người yêu phá thai có phải bị đi tù?
- Chỉ tiêu tăng trưởng GRDP của các địa phương năm 2025 tối thiểu ở mức 8-10%
TÌM KIẾM BÀI VIẾT

